- Статус наличия на складеНа складе
- Способ применения и дозыПрепарат Акласта®, раствор для инфузий, вводят внутривенно инфузионно. Введение препарата следует проводить с помощью клапанной инфузионной системы, обеспечивающей постоянную скорость инфузии, в течение не менее 15 мин. Перед введением препарата Акласта® следует обеспечить адекватную гидратацию пациента. Это особенно важно для пациентов пожилого возраста (≥65 лет), а также для пациентов, получающих терапию диуретическими средствами. Для лечения постменопаузального остеопороза у женщин и остеопороза у мужчин рекомендуемая доза препарата Акласта® составляет 5 мг (содержимое одного флакона препарата - 100 мл раствора) внутривенно 1 раз в год. При недостаточном потреблении кальция и витамина D с пищей следует дополнительно применять препараты кальция и витамина D. Для профилактики последующих переломов у пациентов с переломами проксимального отдела бедренной кости рекомендуемая доза препарата Акласта составляет 5 мг (содержимое одного флакона препарата - 100 мл раствора) внутривенно 1 раз в год. Пациентам с недавним (до 90 дней) переломом проксимального отдела бедренной кости рекомендуется за 2 недели до первой инфузии препарата Акласта® принять однократно витамин D в высокой дозе (от 50 000 до 125 000 ME перорально или внутримышечно). При однократном применении препарата Акласта® пациентам рекомендовано в течение 14 дней до инфузии ежедневно принимать внутрь препараты кальция (1000 мг в сутки и витамина D (800 ME в сутки). После инфузии препарата Акласта® в течение года пациентам также следует принимать препараты кальция и витамина D. Для профилактики последующих переломов у пациентов с переломами проксимального отдела бедренной кости первую инфузию препарата следует проводить через 2 и более недель после операции. Для лечения остеопороза, вызванного применением глюкокортикостероидов, рекомендуемая доза препарата Акласта® составляет 5 мг (содержимое одного флакона препарата - 100 мл раствора) внутривенно 1 раз в год. При недостаточном потреблении кальция и витамина D с пищей у пациентов с остеопорозом следует дополнительно применять препараты кальция и витамина D. Для профилактики постменопаузального остеопороза рекомендуемая доза препарата Акласта® составляет 5 мг (содержимое одного флакона препарата - 100 мл раствора) внутривенно 1 раз в 2 года. Для принятия решения о необходимости проведения повторной инфузии следует ежегодно проводить повторную оценку риска возникновения переломов и оценку клинического ответа на терапию. Для профилактики постменопаузального остеопороза очень важно достаточное поступление в организм кальция и витамина D. В случае их недостаточного потребления с пищей, рекомендуется дополнительный прием препаратов кальция и витамина D. Для лечения костной болезни Педжета рекомендуется однократное введение 5 мг препарата Акласта® внутривенно. Костная болезнь Педжета характеризуется высокой активностью обмена костной ткани. Вследствие быстрого наступления эффекта в отношении костного обмена, после применения препарата Акласта®, в течение первых 10 дней после инфузии, может развиваться преходящая гипокальциемия. На фоне применения препарата Акласта® следует обеспечить достаточное потребление витамина D.. В добавление к этому, строго рекомендовано принимать адекватную дозу кальция (как минимум по 500 мг элементарного кальция 2 раза в сутки) как минимум в течение первых 10 дней после введения препарата Акласта®. Повторное лечение препаратом Акласта® у пациентов с костной болезнью Педжета После однократного применения препарата Акласта® при костной болезни Педжета у пациентов отмечалась продолжительная (около 7,7 лет в среднем) ремиссия. Так как костная болезнь Педжета является хроническим заболеванием, то рекомендуется повторное применение препарата. Повторное применение препарата при болезни Педжета состоит во внутривенном его введении в дозе 5 мг через один год или более от начала лечения. Интервал между введениями препарата Акласта® должен определяться индивидуально на основании эффективности лечения и результатов определения концентрации щелочной фосфатазы, которое следует проводиться каждые 6-12 месяцев. При отсутствии клинических признаков ухудшения состояния, таких как, боль в костях и симптомы компрессии, и/или рентгенологических признаков прогрессирования заболевания, следующая инфузия препарата Акласта® может быть проведена не ранее, чем через 12 месяцев после первой. Продолжительность терапии Оптимальная продолжительность терапии препаратом при долгосрочном применении не определена. У всех пациентов, получающих препарат, периодически следует проводить оценку ответа на терапию и необходимости дальнейшего продолжения лечения с учетом терапевтического эффекта, риска переломов и сопутствующих заболеваний. У пациентов с низким риском переломов следует рассмотреть возможность отмены препарата после первых трех лет его применения, в то же время у пациентов с высоким риском следует рассмотреть возможность продолжения регулярной терапии. У прекративших лечение пациентов следует проводить повторную оценку риска переломов 1 раз в 2-3 года и при необходимости возобновлять лечение. Пациенты с нарушениями функции почек Применение препарата у пациентов с клиренсом креатинина < 35 мл/мин противопоказано. У пациентов с клиренсом креатинина ≥35 мл/мин не требуется коррекции дозы препарата. Пациенты с нарушениями функции печени Пациентам с нарушениями функции печени не требуется коррекции дозы препарата. Пациенты пожилого возраста (≥65 лет) Коррекции дозы препарата не требуется, так как биодоступность, распределение и выведение препарата у пациентов различных возрастов имеют сходный характер. Указания по использованию препарата При подготовке и проведении инфузии следует соблюдать правила асептики. До введения препарата Акласта® следует визуально оценить качество и цвет раствора. Препарат нельзя применять при изменении цвета или появлении нерастворившихся видимых частиц. Препарат Акласта® не следует смешивать или вводить вместе с какими-либо другими препаратами. Нельзя допускать контакта препарата Акласта® с какими-либо растворами, содержащими кальций или любые другие двухвалентные катионы. Для введения препарата всегда следует использовать отдельную систему для инфузий. Неиспользованный раствор препарата Акласта®, оставшийся во флаконе, применять нельзя. Раствор препарата Акласта® желательно использовать непосредственно после вскрытия флакона. Неиспользованный сразу раствор можно хранить в холодильнике при температуре от +2 до + 8 °С не более 24 часов. В случае если раствор охлажден, перед введением его следует выдержать в помещении до достижения комнатной температуры.
- ПроизводительФрезениус Каби Австрия ГмбХ/Лек Фармасью
- Рецепт1
- Срок годности2027-12-31
- Состав1 флакон содержат: действующее вещеставо: золедроновой кислоты моногидрат - 5,33 мг (эквивалентно золедроновой кислоте безводной - 5,00 мг); вспомогательные вещества: маннитол - 4950,00 мг, натрия цитрат дигидрат - 30,00 мг, вода для инъекций до 100 мл (приблизительно 101,45 г)
- Форма выпускараствор для инфузий
- Тип препараталекарственный препарат
- Органы и системыопорно-двигательная система
- Показания к применению
- постменопаузальный остеопороз (для снижения риска переломов бедренной кости, позвонков и внепозвоночных переломов, для увеличения минеральной плотности кости);
- профилактика последующих (новых) остеопоротических переломов у мужчин и женщин с переломами проксимального отдела бедренной кости;
- остеопороз у мужчин;
- профилактика и лечение остеопороза, вызванного применением глюкокортикостероидов;
- профилактика постменопаузального остеопороза (у пациенток с остеопенией);
- костная болезнь Педжета.
- Противопоказания-Повышенная чувствительность к золедроновой кислоте или к любому другому компоненту препарата или к любым бисфосфонатам. -Тяжелые нарушения минерального обмена, включая гипокальциемию. -Беременность, период грудного вскармливания. -Возраст до 18 лет (т.к. безопасность и эффективность применения препарата Акласта® у пациентов данной категории (дети и подростки) не изучались). -Нарушения функции почек тяжелой степени (клиренс креатинина <35 мл/мин). С осторожностью: Следует соблюдать осторожность при применении препарата Акласта®: -у пациентов с нарушением функции почек легкой и средней степени тяжести; -у пациентов в состоянии тяжелой дегидратации; -у пациентов с сопутствующими онкологическими заболеваниями и химиотерапией в анамнезе; -у пациентов с полным или неполным сочетанием бронхиальной астмы, рецидивирующего полипоза носа и околоносовых пазух и непереносимости ацетилсалициловой кислоты или других нестероидных противовоспалительных препаратов (в т.ч. в анамнезе); -при одновременном применении с препаратами, способными оказывать значимое влияние на функцию почек (например, с антибиотиками-аминогликозидами или диуретическими средствами, вызывающими дегидратацию). Если у Вас одно из перечисленных заболеваний (состояний) перед приемом препарата обязательно проконсультируетесь с врачом. Применение при беременности и в период грудного вскармливания: Применение препарата Акласта® во время беременности противопоказано. Препарат Акласта® может оказывать неблагоприятное воздействие на плод. В исследованиях у животных выявлено токсическое воздействие на репродуктивную функцию. Нет данных о применении препарата во время беременности у человека. При возникновении беременности во время терапии бисфосфонатами возможен риск возникновения внутриутробных пороков развития плода (например, аномалий развития скелета и других аномалий внутриутробного развития). Зависимость риска от величины временного промежутка между прекращением терапии бисфосфонатами и моментом зачатия, пути введения и особенностей конкретного препарата неизвестна. Пациентки репродуктивного возраста должны быть предупреждены о необходимости применять надежные методы контрацепции во время лечения препаратом Акласта®. Неизвестно, проникает ли золедроновая кислота в грудное молоко. Применение препарата Акласта® в период грудного вскармливания противопоказано. В исследованиях у животных золедроновая кислота подавляла фертильность в дозе 0,1 мг/кг в сутки. Нет данных о влиянии золедроновой кислоты на фертильность у человека.
- Побочные действияЛечение различных видов остеопороза, костной болезни Педжета, профилактика остеопороза, вызванного применением глюкокортикостероидов, профилактика последующих переломов у мужчин и женщин с переломами проксимального отдела бедренной кости При внутривенном введении 5 мг препарата Акласта® 1 раз в год для лечения постменопаузального остеопороза у женщин, остеопороза у мужчин, для профилактики последующих переломов у мужчин и женщин с переломами проксимального отдела бедренной кости, для профилактики и лечения остеопороза, вызванного применением глюкокортикостероидов и для лечения костной болезни Педжета большинство нежелательных реакций (НР) были слабо или умеренно выраженными. После внутривенного введения препарата Акласта® у данных пациентов наиболее часто наблюдались следующие НР длительностью обычно не более 3-х дней ("постдозовые" симптомы): лихорадка (18,1%), миалгия (9,4%), гриппоподобный синдром (7,8%), артралгии (6,8%), головная боль (6,5%). Большинство вышеназванных НР, отмечавшихся в течение 3-х дней после введения препарата, были слабо или умеренно выраженными. При повторном введении препарата частота данных НР значительно уменьшалась. Выраженность постинфузнонных нежелательных явлений, развивающихся в течение 3 дней после инфузии, может быть уменьшена применением парацетамола или ибупрофена сразу после инфузии препарата Акласта® (см раздел «Особые указания»). Ниже представлены НР, связанные (по мнению лечащих врачей) с применением препарата для лечения различных видов остеопороза, костной болезни Педжета, профилактики остеопороза, вызванного применением глюкокортикостероидов, и для профилактики новых переломов у мужчин и женщин с переломами проксимального отдела бедренной кости. HP сгруппированы в соответствии с классификацией органов и систем органов MedDRA. В пределах каждой группы органов и систем органов HP перечислены в порядке уменьшения частоты встречаемости. Для оценки частоты использованы следующие критерии: очень часто (≥1/10); часто (≥1/100, < 1/10); нечасто (≥1/1 000, < 1/100); редко (≥1/10 000, < 1/1 000); очень редко (< 1/10 000); включая отдельные сообщения. Инфекционные и паразитарные заболевания: нечасто - грипп, назофарингит. Нарушения со стороны крови и лимфатической системы: нечасто - анемия. Нарушения со стороны обмена веществ и питания: нечасто - снижение аппетита. Нарушения психики: нечасто - бессонница. Нарушения со стороны нервной системы: часто - головная боль, головокружение; нечасто - заторможенность*, парестезия, сонливость, тремор, обморок. Нарушения со стороны органа зрения: нечасто - конъюнктивит, боль в глазах; редко - увеит*, эписклерит, ирит. Нарушения со стороны органа слуха и лабиринтные нарушения: нечасто - вертиго. Нарушения со стороны сосудов: нечасто - повышение артериального давления, внезапное покраснение лица. Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: нечасто - одышка*, кашель. Нарушения со стороны пищеварительной системы: часто - тошнота, рвота, диарея; нечасто - диспепсия*, боль в верхних отделах живота, боль в животе*, гастроэзофагеальный рефлюкс, запор, сухость во рту, эзофагит*. Нарушения со стороны кожи и подкожных тканей: нечасто - кожная сыпь, гипергидроз*, кожный зуд, эритема. Нарушения со стороны скелетно-мышечной и соединительной ткани: часто - артралгия*, миалгия*, боль в костях, боль в спине и конечностях; нечасто - боль в области шеи, скованность в мышцах, отек в области суставов*, мышечные спазмы, боль в области грудной клетки* мышечно-скелетного происхождения, скелетно-мышечная боль, скованность суставов*, артрит, мышечная слабость. Нарушения со стороны почек и мочевыводящих путей: нечасто - повышение концентрации креатинина в крови, поллакиурия, протеинурия. Общие расстройства и нарушения в месте введения: очень часто - лихорадка; часто - гриппоподобный синдром, озноб, повышенная утомляемость*, астения, боль*, общее недомогание; нечасто - периферические отеки, жажда*, реакции острой фазы*, некардиогенная боль в груди (не связанная с заболеваниями сердца). В отдельных исследованиях наиболее часто были отмечены следующие HP: очень часто - миалгия, артралгия, повышенная утомляемость, боль; часто - заторможенность, одышка, диспепсия, эзофагит, боль в животе, гипергидроз, скованность в мышцах, отек в области суставов, боль в области грудной клетки мышечно- скелетного происхождения, скованность в суставах, снижение аппетита, жажда, реакции острой фазы; нечасто - увеит. В ходе отдельных исследований были зарегистрированы HP, частота развития которых в группе применения препарата Акласта® была ниже, чем у пациентов, получавших плацебо. Нарушения со стороны сердца: фибрилляция предсердий, ощущение сердцебиения. Нарушения со стороны органа зрения: покраснение глаз. Нарушения со стороны пищеварительной системы: гастрит (у пациентов, получающих глюкокортикостероиды), зубная боль. Общие расстройства и нарушения в месте введения: реакции в месте введения. Лабораторные и инструментальные данные: повышение концентрации С-реактивного белка. Нарушения со стороны обмена веществ и питания: гипокальциемия. Нарушения со стороны нервной системы: дисгевзия. Профилактика постменопаузального остеопороза При применении препарата Акласта® для профилактики постменопаузального остеопороза (ПМО) общий профиль безопасности препарата был сравним с таковым при лечении ПМО, за исключением НР, возникавших в течение 3-х дней после инфузии: боль, лихорадка, озноб, миалгия, тошнота, головная боль, повышенная утомляемость, головокружение, артралгия, частота которых была выше у пациенток, получавших препарат для профилактики ПМО. Большинство этих НР были легкой или средней степени выраженности и проходили в течение 3-х дней после появления. При повторном введении препарата частота встречаемости данных НР значительно уменьшалась. Ниже представлены НР, связанные с применением препарата для профилактика ПМО (по мнению лечащих врачей): 1) НР, отмечавшиеся более чем один раз при введении препарата Акласта® для профилактики ПМО и не зарегистрированные при применении препарата Акласта® для лечения различных видов остеопороза, костной болезни Педжета, профилактики остеопороза, вызванного применением глюкокортикостероидов, и для профилактики новых переломов у мужчин и женщин с переломами проксимального отдела бедренной кости; 2) НР, частота которых была выше у женщин, получавших препарат для профилактики ПМО (по сравнению с другими категориями пациентов). Частота развития данных НР, оценивалась следующим образом: очень часто (≥1/10); часто (≥1/100, < 1/10); нечасто (≥1/1 000, < 1/100). Нарушения со стороны обмена веществ и питания: часто - снижение аппетита. Нарушения психики: нечасто - тревога. Нарушения со стороны нервной системы: очень часто - головная боль; часто - тремор, заторможенность; нечасто - гипестезия, дисгевзия. Нарушения со стороны органа зрения: часто - конъюнктивит, боль в глазах, ирит; нечасто - нечеткое зрение. Нарушения со стороны пищеварительной системы: очень часто - тошнота; часто - боль в животе, боль в верхних отделах живота, запор. Нарушения со стороны кожи и подкожной клетчатки: часто - повышенное потоотделение в ночное время. Нарушения со стороны скелетно-мышечной и соединительной ткани: очень часто - миалгия; часто - скелетно-мышечная боль, спазм мышц, боль в области грудной клетки мышечно-скелетного происхождения, боль в области челюсти, боль в области шеи; нечасто - боль в боку. Общие расстройства и нарушения в месте введения: очень часто - боль, озноб; часто - периферические отеки, реакции в месте введения препарата, некардиогенная боль в области грудной клетки. Описание отдельных нежелательных реакций Нарушения функции почек При внутривенном введении бисфосфонатов, включая золедроновую кислоту, отмечались случаи нарушения функции почек с повышением концентрации креатинина крови, и в редких случаях, с острой почечной недостаточностью. Нарушения функции почек после однократного применения золедроновой кислоты наблюдались у пациентов с предшествующим нарушением функции почек, либо при наличии дополнительных факторов риска (например, пожилой возраст, онкологические пациенты, получающие химиотерапию, сопутствующее применение нефротоксических или диуретических препаратов, или тяжелая дегидратация) с преобладанием у пациентов, получавших препарат в дозе 4 мг каждые 3-4 недели. При этом у пациентов с нарушениями функции почек или любым из вышеперечисленных факторов риска почечная недостаточность, требующая проведения гемодиализа или приводящая к летальному исходу, встречалась редко. Следует соблюдать осторожность при применении препарата Акласта® у пациентов с сопутствующими онкологическими, получающим химиотерапию, вследствие повышенного риска развития почечной недостаточности. При терапии препаратом Акласта® в течение 3-х лет у пациенток с постменопаузальным остеопорозом частота повышения концентрации креатинина в плазме крови и развития нарушения функции почек не отличалась от таковой при применении плацебо. У пациенток, получавших препарат Акласта®, несколько чаще наблюдалось преходящее повышение концентрации креатинина крови в течение 10 дней после инфузии по сравнению с плацебо (1,8% и 0,8%, соответственно). При применении препарата Акласта® в течение 2-х лет у мужчин с остеопорозом частота изменения клиренса креатинина и развития нарушений функции почек была сходной с таковой в группе приема алендроновой кислоты. У пациентов с остеопорозом, вызванном применением глюкокортикостероидов, на фоне терапии препаратом Акласта® частота изменения клиренса креатинина и развития нарушений функции почек была сходной с таковой в группе приема ризедроновой кислоты. При применении препарата у пациентов с переломами бедренной кости частота изменения клиренса креатинина и развития нарушений функции почек была сходной с таковой в группе плацебо. При применении препарата у пациентов для профилактики постменопаузального остеопороза частота изменения клиренса креатинина и развития нарушений функции почек была сходной с таковой в группе плацебо. Гипокальциемия У пациенток с постменопаузальным остеопорозом на фоне применения препарата Акласта® в 0,2% случаев отмечалось снижение содержания кальция (<1,87 ммоль/л) в сыворотке крови, клинических признаков гипокальциемии при этом не наблюдалось. При применении препарата у пациентов с переломами бедренной кости, при мужском остеопорозе и остеопорозе, вызванном приемом глюкокортикостероидов, не было пациентов, которым потребовалась срочная терапия при содержании кальция в плазме крови <1,87 ммоль/л. При применении препарата у пациентов для профилактики постменопаузального остеопороза одной пациентке потребовалась срочная терапия при концентрации кальция в плазме крови <1,87 ммоль/л. У пациентов с болезнью Педжета приблизительно в 1% случаев обнаруживалась преходящая гипокальциемия, сопровождавшаяся клиническими проявлениями. Реакции в месте введения препарата При применении препарата Акласта® у пациенток с постменопаузальным остеопорозом в 0,7% случаев отмечались покраснение, отечность и/или болезненность в месте введения. У пациентов с переломами бедренной кости частота развития местных реакций была сравнимой с таковой в группе плацебо. При лечении остеопороза у мужчин частота развития реакций в месте введения препарата Акласта® составляла 2,6% (по сравнению с 1,4% в группе приема алендроновой кислоты). У пациентов с остеопорозом, вызванным применением глюкокортикостероидов, не отмечалось реакций в месте введения препарата. При применении препарата для профилактики постменопаузального остеопороза частота развития реакций в месте введения препарата Акласта® составляла 1,1% (по сравнению с 2,0% в группе плацебо). Остеонекроз челюсти Случаи развития остеонекроза (наиболее часто - остеонекроз челюсти) имели место в основном у онкологических пациентов, получающих лечение бисфосфонатами (включая золедроновую кислоту - нечасто), в большинстве случаев после экстракции зуба или иных стоматологических манипуляций. У большинства пациентов были симптомы местного инфекционно-воспалительного процесса, включая остеомиелит. Известными факторами риска остеонекроза челюсти являются онкологические заболевания, сопутствующая терапия (например, химиотерапия, антиангиогенные препараты, радиотерапия, глюкокортикостероидов) и сопутствующие заболевания (например, анемия, коагулопатии, инфекции, предшествующая стоматологическая патология). Хотя причинно-следственная связь остеонекроза челюсти с применением бисфосфонатов не установлена, следует избегать стоматологических операций, поскольку сроки восстановления после указанных операций могут увеличиваться (см. раздел «Особые указания»). В клинических исследованиях у пациентов с остеопорозом случай остеонекроза челюсти имел место у 1 пациентки, получавшей препарат Акластам, и у 1 пациентки, получавшей плацебо. В обоих случаях отмечалось разрешение процесса. При применении препарата Акласта® у пациентов с переломами бедренной кости, при мужском остеопорозе и остеопорозе, вызванном приемом глюкокортикостероидов, а также при применении препарата для профилактики постменопаузального остеопороза не отмечалось случаев развития остеонекроза челюсти. Фибрилляции предсердий При применении препарата Акласта® у пациенток с постменопаузальным остеопорозом общая частота развития фибрилляции предсердий на фоне терапии препаратом Акласта® составляла 2,5% (96 человек из 3862) по сравнению с 1,9% (75 из 3852) у пациентов, не получавших лечение препаратом (группа плацебо). У 1,3% больных (51 пациентка из 3862), получавших препарат Акласта, и у 0,6% (22 пациента из 3852) в группе плацебо данное нежелательное явление было расценено как серьезное. Причина повышения частоты фибрилляции предсердий на фоне терапии препаратом Акласта в данном исследовании не установлена. Повышение частоты фибрилляции предсердий в сравнении с плацебо, отмеченное в данном исследовании, не было обнаружено в других клинических исследованиях золедроновой кислоты. Отдельные сообщения о нежелательных явлениях Во время проведения пострегистрационных исследований были выявлены следующие побочные реакции (поскольку сообщения получены в добровольном порядке от популяции неопределенного размера, достоверно определить частоту развития данных HP не представляется возможным, в связи с чем они классифицированы как частота неизвестна). HP сгруппированы в соответствии с классификацией органов и систем органов MedDRA. В пределах каждой группы органов и систем органов HP указаны в порядке уменьшения их тяжести. Нарушение со стороны органа зрения: склерит, воспаление периорбитальных тканей. Нарушения со стороны иммунной системы: реакции гиперчувствительности, включая анафилактическую реакцию, анафилактический шок, ангионевротический отек, бронхоспазм, крапивницу. Нарушения со стороны обмена веществ и питания: дегидратация (развивающаяся вследствие постинфузионных явлений, таких как лихорадка, рвота и диарея), гипофосфатемия. Нарушения со стороны сосудов: выраженное снижение артериального давления (у пациентов с факторами риска). Нарушения со стороны скелетно-мышечной и соединительной ткани: остеонекроз челюсти. Нарушения со стороны почек и мочевыводящих путей: нарушения функции почек, включая почечную недостаточность, требующую проведения гемодиализа, или случаи летального исхода* особенно у пациентов с наличием либо почечной патологии в анамнезе, либо дополнительных факторов риска (например, пожилой возраст, сопутствующая терапия нефротоксическими препаратами, диуретическими средствами или при тяжелой дегидратации). Если любые из указанных в инструкции побочных эффектов усугубляются, или Вы заметили любые другие побочные эффекты, не указанные в инструкции, сообщите об этом врачу.
- Способ применения/введенияпарентеральный
- Условия храненияБеречь от детей
- ПередозировкаВ настоящее время не существует достаточно клинических данных о случаях передозировки препаратом. Пациенты, получившие дозу препарата, которая превосходит рекомендуемую, должны находиться под наблюдением врача. При острой передозировке золедроновой кислоты (ограниченные данные) отмечались нарушения функции почек, включая почечную недостаточность, гипокальциемию, гипофосфатемию, гипомагниемию. В случае передозировки препаратом, сопровождающейся клинической симптоматикой (онемение, ощущение покалывания, особенно в области рта, мышечные спазмы и т.д.), показано внутривенное введение растворов, содержащих ионы кальция, магния и фосфаты. При невозможности внутривенного введения препаратов кальция, возможен их пероральный прием.
- Особые указанияВрачу следует проинформировать пациентов об основных проявлениях гипокальциемии и обеспечить регулярное наблюдение пациентов, входящими в группу риска. Терапию препаратом Акласта® у пациентов с костной болезнью Педжета должны проводить только квалифицированные врачи, имеющие опыт лечения данного заболевания. Выраженность послеинфузионных нежелательных явлений, развивающихся в течение 3 дней после инфузии, может быть уменьшена применением парацетамола или ибупрофена сразу после инфузии препарата Акласта®. Золедроновая кислота является действующим веществом как препарата Акласта®, так и препарата Зомета® (препарата для лечения онкологических пациентов), однако данные лекарственные средства не являются взаимозаменяемыми и не должны применяться одновременно. При наличии гипокальциемии перед началом применения препарата Акласта® необходимо провести лечение адекватными дозами кальция и витамина D. Также следует провести терапию других имеющихся нарушений минерального обмена (например, возникающих после операций на щитовидной и паращитовидной железах, при гипопаратиреозе или снижении всасывания кальция в кишечнике) и обеспечить регулярное наблюдение пациентов с гипокальциемией. Нарушения функции почек Для снижения риска развития нарушений со стороны почек следует соблюдать следующие указания: • Препарат противопоказан пациентам с нарушениями функции почек тяжелой степени тяжести (клиренс креатинина <35 мл/мин). • Перед каждым введением препарата необходимо определять клиренс креатинина (например, по формуле Кокрофта-Голта). На фоне терапии препаратом у пациентов, имеющих в анамнезе нарушения функции почек, транзиторное повышение концентрации креатинина в плазме крови может быть выше, чем у пациентов с нормальной функцией почек. При применении препарата Акласта® у пациентов, имеющих факторы риска возникновения нарушений со стороны почек, определение концентрации креатинина в плазме крови должно проводиться регулярно. • Следует соблюдать осторожность при одновременном применении препарата Акласта® с препаратами, способными оказывать значимое влияние на функцию почек (см. раздел "Взаимодействие с другими лекарственными средствами"), • Перед введением препарата Акласта® следует обеспечить адекватную гидратацию организма. Это особенно важно для пациентов в возрасте > 65 лет, а также у пациентов, получающих терапию диуретическими средствами. • Доза препарата при однократной внутривенной инфузии не должна превышать 5 мг, при этом введение препарата Акласта® следует проводить в течение не менее 15 мин. Костно-мышечная боль В пострегистрационных исследованиях применения бисфосфонатов, в том числе препарата Акласта®, были зарегистрированы случаи развития выраженной, в некоторых случаях некупируемой, костно-мышечной, суставной и/или мышечной боли. Указанные симптомы развивались как в первый день лечения препаратом, так и в течение нескольких месяцев после начала терапии. В случае развития тяжелых симптомов следует рассмотреть возможность отмены препарата Акласта®. В большинстве случаев после отмены препарата симптомы регрессировали, однако, после возобновления терапии препаратом Акласта® или другими бисфосфонатами у группы пациентов симптомы возобновлялись. Остеонекроз челюсти Факторами риска развития остеонекроза являются онкологические заболевания, сопутствующая терапия (например, химиотерапия, одновременное применение с препаратами ингибиторами ангиогенеза, лучевая терапия, лечение глюкокортикостероидами) и наличие других сопутствующих заболеваний (например, анемии, коагулопатий, инфекций, заболеваний зубов в анамнезе). Хотя причинно-следственная связь остеонекроза челюсти с приемом бисфосфонатов не установлена, следует избегать стоматологических операций, поскольку сроки восстановления после указанных операций могут увеличиваться. До начала лечения бисфосфонатами необходимо провести стоматологическое обследование и заранее выполнить необходимые профилактические процедуры у пациентов, имеющих факторы риска (онкологические заболевания, химиотерапия, лечение глюкокортикостероидами, несоблюдение гигиены полости рта). Во время лечения золедроновой кислотой целесообразно поддерживать надлежащую гигиену ротовой полости, проходить рутинное обследование у стоматолога и незамедлительно сообщать врачу обо всех симптомах со стороны ротовой полости. При развитии остеонекроза челюсти на фоне терапии бисфосфонатами проведение стоматологических операций может ухудшить состояние пациентов. Нет сведений о том, что прерывание лечения бисфосфонатами до стоматологических вмешательств снижает риск остеонекроза челюсти. Тактика лечения конкретного пациента должна быть основана на индивидуальной оценке соотношения польза/риск. Отмечались случаи возникновения переломов другой локализации (в т.ч., бедренной кости, тазовой кости, коленного сустава, плечевой кости), однако у пациентов, получавших лечение препаратом Акласта®, причинно-следственная связь с приемом препарата не установлена. Отмечались отдельные случаи возникновения бронхоконстрикции у пациентов с полным или неполным сочетанием бронхиальной астмы, рецидивирующего полипоза носа и околоносовых пазух и непереносимости ацетилсалициловой кислоты или других нестероидных противовоспалительных препаратов (в т.ч. в анамнезе) на фоне приема бисфосфонатов. Хотя в клинических исследованиях с участием препарата Акласта® таких случаев отмечено не было, рекомендуется применять препарат с осторожностью у пациентов с полным или неполным сочетанием бронхиальной астмы, рецидивирующего полипоза носа и околоносовых пазух и непереносимости ацетилсалициловой кислоты или других нестероидных противовоспалительных препаратов (в т.ч. в анамнезе). Остеонекроз наружного слухового прохода Зарегистрированы случаи развития остеонекроза наружного слухового прохода при лечении бисфосфонатами, которые наблюдались, в основном, при длительной терапии. Возможными факторами риска развития остеонекроза наружного слухового прохода являются применение глюкокортикостероидных препаратов, химиотерапия и/или такие местные факторы риска как инфекция или травма. Необходимо помнить о возможности развития остеонекроза наружного слухового прохода у пациентов, получающих бисфосфонаты, с симптомами хронической инфекции уха. Атипичные переломы бедренной кости Имеются сообщения о случаях атипичных подвертельных и диафизарных переломов бедренной кости у пациентов, длительно получающих антиостеопоретическую терапию бисфосфонатами. Эти переломы, поперечные или короткие косые, локализуются на любом участке от малого вертела до надмыщелков и возникают, как правило, спонтанно или после незначительной травмы. До обнаружения бедренных переломов пациенты могут на протяжении нескольких недель или месяцев испытывать боль в области бедра или паха. Переломы часто двусторонние, поэтому при диагностировании перелома бедренной кости у пациента, получающего бисфосфонаты, также необходимо обследовать контрлатеральную бедренную кость. Есть сообщения, что данные переломы сопровождаются медленным заживлением (срастанием). Решение об отмене терапии бисфосфонатами у пациентов с подозрением на атипичные переломы бедренной кости должно быть основано на индивидуальной оценке соотношения риска и пользы. Четкая причинно-следственная связь между применением бисфосфонатов и переломами бедренной кости установлена не была, так как атипичные переломы также возникали у пациентов с остеопорозом, которые не получали терапию бисфосфонатами. Все пациенты, получающие терапию бисфосфонатами, включая препарат Акласта®, должны быть информированы о необходимости сообщать о любой боли в области бедра или паха, и любой такой пациент должен быть обследован на наличие у него перелома бедренной кости. Влияние на способность управлять транспортными средствами и другими механизмами: Данных о влиянии препарата Акласта® на способность управлять транспортными средствами и работать с механизмами нет. Однако, в связи с тем, что головокружение является одним из побочных эффектов препарата Акласта®, пациентам следует соблюдать осторожность при выполнении потенциально опасных видов деятельности. При появлении описанного нежелательного явления следует воздержаться от указанных видов деятельности.
- ВзаимодействиеСпециальных исследований по изучению взаимодействия золедроновой кислоты с другими лекарственными средствами не проводилось. Золедроновая кислота не подвергается системному метаболизму и не влияет на изоферменты цитохрома Р450 человека in vitro. Золедроновая кислота характеризуется относительно низкой степенью связывания с белками плазмы (приблизительно 43-55%); лекарственное взаимодействие, обусловленное вытеснением лекарственных веществ с высокой степенью связывания с белками из мест связывания, маловероятно. Золедроновая кислота выводится почками. Следует соблюдать осторожность при одновременном применении препарата Акласта® с препаратами, способными оказывать значимое влияние на функцию почек (например, с антибиотиками-аминогликозидами или диуретическими средствами, вызывающими дегидратацию). У пациентов с нарушениями почечной функции при применении препарата Акласта® совместно с препаратами, которые выводятся преимущественно почками, возможно повышение системного действия данных лекарственных средств. Фармацевтическое взаимодействие и вопросы совместимости Раствор препарата Акласта® несовместим с растворами, содержащими кальций или другие двухвалентные катионы (например, в одной системе для внутривенного капельного введения).
- Владелец регистрационного удостоверенияНовартис Фарма АГ
- ИзготовительFresenius Kabi Austria GmbH
- Страна-производительАвстрия
- Название препаратаАкласта
- Минимальный возраст примененияот 18 лет
- Страна брендаШвейцария
- ФасовщикFresenius Kabi Austria GmbH
- Количество в упаковке1
- УпаковкаРаствор для инфузий 5 мг/100 мл - по 100 мл во флакон. По одному флакону вместе с инструкцией по применению в картонную пачку.
- Вес100
- Совместимость<p>Специальных исследований по изучению взаимодействия золедроновой кислоты с другими лекарственными средствами не проводилось. Золедроновая кислота не подвергается системному метаболизму и не влияет на изоферменты цитохрома P450 человека in vitro.</p> <p>Золедроновая кислота характеризуется относительно низкой степенью связывания с белками плазмы (приблизительно 43-55%); лекарственное взаимодействие, обусловленное вытеснением лекарственных веществ с высокой степенью связывания с белками из мест связывания, маловероятно.</p> <p>Золедроновая кислота выводится почками. Следует соблюдать осторожность при одновременном применении препарата Акласта® с препаратами, способными оказывать значимое влияние на функцию почек (например, с антибиотиками-аминогликозидами или диуретическими средствами, вызывающими дегидратацию).</p> <p>У пациентов с нарушениями почечной функции при применении препарата Акласта® совместно с препаратами, которые выводятся преимущественно почками, возможно повышение системного действия данных лекарственных средств.</p> <p><em>Фармацевтическое взаимодействие и вопросы совместимости</em></p> <p>Раствор препарата Акласта® несовместим с растворами, содержащими кальций или другие двухвалентные катионы (например, в одной системе для внутривенного капельного введения).</p>
- Нижний порог температуры2
- Верхний порог температуры25
- Показания-постменопаузальный остеопороз (для снижения риска переломов бедренной кости, позвонков и внепозвоночных переломов, для увеличения минеральной плотности кости); -профилактика последующих (новых) остеопоротических переломов у мужчин и женщин с переломами проксимального отдела бедренной кости; -остеопороз у мужчин; -профилактика и лечение остеопороза, вызванного применением глюкокортикостероидов; -профилактика постменопаузального остеопороза (у пациенток с остеопенией); -костная болезнь Педжета.
- Выберите товары и добавьте их в корзину;
- Перейдите в раздел «Корзина» и нажмите «Оформить заказ»;
- Укажите ваши данные;
- Выберите способ доставки и укажите адрес;
- Выберите способ оплаты;
- Нажмите "Оформить заказ";
- В зависимости от варианта оплаты - оплатите заказ или дождитесь звонка оператора (при самовывозе);
Если возникли вопросы с оформлением заказа, пишите менеджерам в онлайн-чат.
Оплачивайте покупки удобным способом. В интернет-магазине доступно 4 варианта оплаты:
- Картой Онлайн. Оплата производится через защищенное соединение на странице банка. Мы не видим и не сохраняем данные Вашей карты. Сразу после оплаты вы получите чек об оплате на электронную почту.
- Картой или электронными деньгами через Яндекс.Кассу.
- Безналичный расчет (для юр. лиц)
- Наличными или картой при самовывозе из нашей аптеки в гор. Самара.
- Наличными Курьеру при доставке по Самаре.
- Лекарства можно получить и оплатить СТРОГО в нашей аптеке в гор. Самара - Ул. Солнечная, д. 16, оф. 2. Если у Вас в корзине будут лекарства, вы не сможете выбрать другой вариант доставки, а при выборе города, отличного от Самары, у Вас не будет никаких вариантов доставки.
-
Курьерская служба DPD. Только для разрешенных, согласно законодательства РФ, к доставке товаров. Доставка по России курьерской службой DPD. 1-2 дня Европейская часть России. До 5 дней Сибирь. До 12 дней Дальний Восток.
Мы доставим Ваш заказ за несколько дней по всей территории России курьерскими службами на дом или в пункт выдачи заказов. Цена доставки высчитывается при оформлении заказа автоматически.
Стоимость доставки:
- В пункты самовывоза: от 210 рублей (от 1 рабочего дня)
- Курьером: от 310 рублей (от 1 рабочего дня)
-
Почта России.Самая большая география доставки и самая низкая стоимость доставки, при этом сроки и качество обслуживания в последнее время заметно улучшились.
В крупных городах доступны варианты доставки "Курьер Онлайн" и "Посылка Онлайн" - самые быстрые сроки доставки и самая низкая стоимость.
Все крупные центральные города России от 210 рублей курьером на дом, либо 160 рублей в отделение.
Также Почта России доставляет в самые отдаленные города.
-
Курьерская доставка по гор. Самара
Вы можете заказать доставку товара с помощью курьера, который прибудет по указанному адресу ежедневно с 9.00 до 21.00. После поступления товара на склад, мы свяжемся с вами и предложим выбрать удобное время доставки. Уточним адрес.
Вы вскрываете упаковку при курьере, осматриваете на целостность и соответствие указанной комплектации.
Стоимость доставки начинается от 249 рублей, в зависимости от адреса доставки.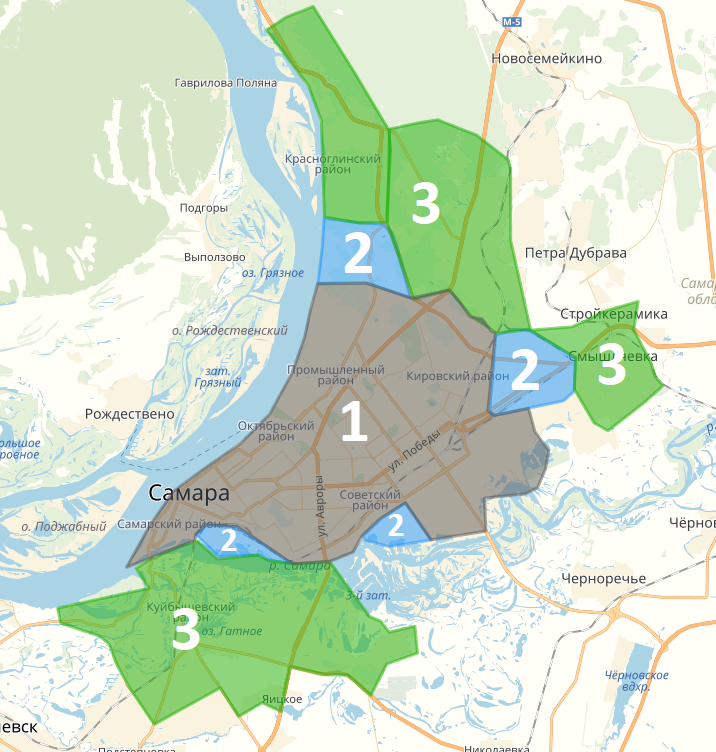
Зона 1 - 249 руб.
Зона 2 - 299 руб.
Зона 3 - 449 руб
Мы доставляем товары (кроме лекарств и товаров, требующих специальные условия перевозки) по всей России в короткие сроки. Рассчитать стоимость доставки вы можете на этой странице, нажав на кнопку "Рассчитать доставку".
Мы работаем с юридическими лицами по безналичному расчету. Предоставляем при этом все отчетные документы и сертификаты качества товара. Оформить заказ как юр. лицо, вы можете на странице оформления заказа.
Приобретать товар у нас очень выгодно - наши цены одни из самых низких во всем интернете. При этом, мы гарантируем, что вы получите товар высокого качества, ведь мы производим закупки у производителей, либо у федеральных фармацевтических дистрибьютеров.