- Статус наличия на складеНа складе
- Способ применения и дозыЖенщины с детородным потенциалом (контрацепция у мужчин и женщин) Женщины При применении препарата Микофенолата мофетил следует избегать наступления беременности. Таким образом, пациенткам с детородным потенциалом необходимо использовать как минимум один надежный метод контрацепции (см. раздел «Противопоказания») до начала терапии, во время терапии и в течение шести недель после прекращения терапии препаратом Микофенолата мофетил, если они не выбрали воздержание от половой жизни в качестве метода контрацепции. Предпочтительно использовать два дополняющих друг друга метода контрацепции одновременно. Мужчины Клинические данные о воздействии ММФ на отцовский организм ограничены и не содержат свидетельств о повышенном риске развития врожденных пороков или выкидыша вследствие приема ММФ отцом. МФК является мощным тератогеном. Неизвестно, присутствует ли МФК в сперме. Согласно расчетам, основанным на результатах исследований у животных, максимальное количество МФК, которое потенциально может быть передано женщине, настолько мало, что его влияние будет маловероятным. Исследования у животных показали генотоксичность ММФ в концентрациях, лишь немного превышающих терапевтические экспозиции у человека, поэтому риск генотоксического действия на сперматозоиды не может быть полностью исключен. Таким образом, рекомендуются следующие предупредительные меры: ведущим половую жизнь пациентам-мужчинам или половым партнершам пациентов-мужчин следует использовать надежные методы контрацепции во время лечения пациента-мужчины ММФ и как минимум в течение 90 дней после прекращения терапии. Пациентам-мужчинам с репродуктивным потенциалом должно быть известно о потенциальных рисках зачатия ребенка; их следует обсудить с квалифицированным медицинским специалистом. Беременность Применение ММФ противопоказано во время беременности, за исключением случаев отсутствия подходящей альтернативной терапии для профилактики отторжения трансплантата. Не следует начинать лечение до получения отрицательного результата теста на беременность, чтобы исключить непреднамеренное применение препарата во время беременности. Перед началом терапии пациенток с детородным потенциалом необходимо проинформировать о повышенном риске спонтанных абортов и врожденных пороков развития, и направить на консультацию по поводу предотвращения и планирования беременности. Перед началом терапии препаратом Микофенолата мофетил у пациенток с детородным потенциалом должны быть получены отрицательные результаты 2-х тестов на беременность при использовании методов анализа сыворотки или мочи с чувствительностью не менее 25 мМЕ/мл для исключения непреднамеренного воздействия ММФ на эмбрион. Рекомендуется проведение второго теста через 8-10 дней после первого теста. В случае трансплантации от умерших доноров, если возможность проведения двух отдельных тестов на беременность с интервалом 8-10 дней отсутствует (ввиду временных ограничений доступности трансплантата), первый тест на беременность должен быть проведен непосредственно перед началом терапии, а второй через 8-10 дней после первого. Повторные тесты на беременность должны проводиться в зависимости от клинических показаний (например, после сообщения о нарушении правил контрацепции). Результаты всех тестов на беременность необходимо обсудить с пациенткой. Пациентки должны быть проинформированы, что в случае наступления беременности им необходимо незамедлительно проконсультироваться с лечащим врачом. ММФ представляет собой вещество, оказывающее мощное тератогенное воздействие на человека, повышающее риск спонтанных абортов и возникновения врожденных пороков развития при его применении во время беременности: • Частота спонтанных абортов у пациенток, получавших ММФ, составила 45-49 %, в то время как у пациенток, получавших лечение другими иммунодепрессантами после трансплантации солидных органов, такой риск составляет 12-33 %. • Согласно опубликованным данным у 23-27 % живых новорожденных, которые подверглись воздействию ММФ в период внутриутробного развития, наблюдались врожденные пороки развития (по сравнению с частотой пороков развития у живых новорожденных 2-3% в общей популяции и приблизительно 4-5% у пациентов, перенесших трансплантацию солидных органов, получающих лечение другими иммунодепрессантами (не ММФ). У детей пациенток, получавших лечение ММФ в комбинации с другими иммунодепрессантами во время беременности, при пострегистрационном применении наблюдались врожденные пороки развития, включая множественные пороки развития. Наиболее часто отмечались следующие пороки развития: • аномалии развития уха (например, аномалия формы или отсутствие наружного уха), атрезия наружного слухового прохода (среднего уха); • пороки развития лица, такие как расщепленная губа, расщепленное небо, микрогнатия и гипертелоризм глазниц; • аномалии развития глаза (например, колобома); • аномалии сердца, такие как дефект межпредсердной и межжелудочковой перегородок; • пороки развития пальцев (например, полидактилия, синдактилия); • трахеоэзофагеальные пороки развития (например, атрезия пищевода); • пороки развития нервной системы (такие как незаращение дужек позвонков); • пороки развития почек. Отдельные сообщения о следующих пороках развития: • микрофтальм; • врожденная киста сосудистого сплетения; • агенез прозрачной перегородки; • агенез обонятельного нерва. Исследования на животных показали репродуктивную токсичность (см. раздел подраздел «Доклинические данные по безопасности» раздела «Фармакологические свойства»). Лактация Было показано, что у лактирующих крыс ММФ выделяется с молоком. Неизвестно, выделяется ли ММФ с грудным молоком у женщин. Препарат Микофенолата мофетил противопоказан в период грудного вскармливания в связи с риском развития серьезных нежелательных реакций на ММФ у детей, находящихся на грудном вскармливании (см. раздел «Противопоказания»). Фертильность ММФ не оказывал воздействия на фертильность самцов крысы при пероральном введении в дозах до 20 мг/кг/сутки. Системная экспозиция при такой дозе в 2-3 раза превышала клиническую экспозицию, наблюдаемую при приеме препарата в рекомендованной клинической дозе 2 г/сутки у пациентов после трансплантации почки, и в 1.3-2 раза превышала клиническую экспозицию, наблюдаемую при приеме препарата в рекомендованной клинической дозе 3 г/сутки у пациентов после трансплантации сердца. В исследованиях фертильности и репродуктивности самок крыс пероральное введение ММФ в дозе 4,5 мг/кг/сутки вызывало пороки развития (в том числе анофтальмию, агнатию и гидроцефалию) в первом поколении потомства без какого-либо токсического действия на мать. Системная экспозиция при такой дозе приблизительно в 0,5 раза превышала клиническую экспозицию, наблюдаемую при приеме препарата в рекомендованной клинической дозе 2 г/сутки у пациентов после трансплантации почки, и приблизительно в 0,3 раза превышала клиническую экспозицию, наблюдаемую при приеме препарата в рекомендованной клинической дозе 3 г/сутки у пациентов после трансплантации сердца. В последующих поколениях потомства влияния на фертильность или репродуктивность самок не отмечалось
- ПроизводительОЗОН ООО
- Рецепт1
- Срок годности2029-01-31
- Состав1 таблетка содержит: Действующее вещество: микофенолата мофетил - 500,000 мг. Вспомогательные вещества: целлюлоза микрокристаллическая (МКЦ-101) - 87,400 мг; повидон-К25 - 39,600 мг; кроскармеллоза натрия - 26,400 мг; магния стеарат - 6,600 мг. Состав оболочки: поливиниловый спирт - 8,000 мг; титана диоксид - 7,124 мг, макрогол-4000 - 4,876 мг.
- Форма выпускатаблетки, покрытые пленочной оболочкой
- Показания к применению
Микофенолата мофетил применяют в виде комбинированной терапии с циклоспорином и глюкокортикостероидами.
Таблетки, покрытые пленочной оболочкой 250 мг
Взрослые и дети с площадью поверхности тела > 1.25 м² (примерный детский возраст старше 12 лет):
- профилактика острого отторжения трансплантата у пациентов после аллогенной пересадки почки.
Взрослые:
- профилактика острого отторжения трансплантата у пациентов после аллогенной пересадки сердца;
- профилактика острого отторжения трансплантата у пациентов после аллогенной пересадки печени.
Таблетки, покрытые пленочной оболочкой 500 мг
Взрослые и дети с площадью поверхности тела > 1.5 м² (примерный детский возраст старше 14 лет):
- профилактика острого отторжения трансплантата у пациентов после аллогенной пересадки почки.
Взрослые:
- профилактика острого отторжения трансплантата у пациентов после аллогенной пересадки сердца;
- профилактика острого отторжения трансплантата у пациентов после аллогенной пересадки печени.
- Противопоказания• Гиперчувствительность к ММФ, МФК или другим компонентам препарата. • Дефицит гипоксантингуанинфосфорибозилтрансферазы (редкое генетическое заболевание, обусловленное наследственным дефицитом гипоксантингуанинфосфорибозилтрансферазы - синдромы Леша-Найена и Келли-Зигмиллера). • Одновременный прием с азатиоприном (оба препарата угнетают костный мозг, их одновременный прием не изучался). • Дети с площадью поверхности тела < 1,25 м2 (примерный детский возраст до 12 лет) для препарата в дозировке 250 мг. • Дети с площадью поверхности тела < 1,5 м2 (примерный детский возраст до 14 лет) для препарата в дозировке 500 мг. • Беременность (применение ММФ противопоказано во время беременности вследствие его мутагенного и тератогенного потенциала). • Женщины детородного потенциала, не использующие высокоэффективные методы контрацепции. • Женщины детородного потенциала без предварительного проведения теста на беременность, чтобы исключить непреднамеренное применение препарата при беременности. • Период грудного вскармливания.
- Побочные действияРезюме профиля безопасности Среди наиболее частых и/или серьезных нежелательных реакций, связанных с применением ММФ в комбинации с циклоспорином и глюкокортикостероидами, были диарея (до 52,6%), лейкопения (до 45,8%), бактериальные инфекции (до 39,9%) и рвота (до 39,1%). Также существуют данные о повышении частоты развития некоторых типов инфекций (см. раздел «Особые указания»). Табличное резюме нежелательных реакций Нежелательные реакции, наблюдавшиеся в ходе клинических исследований и пострегистрационного применения ММФ (см. таблицу ниже), сгруппированы по классам систем органов медицинского словаря для нормативно-правовой деятельности (MedDRA) в соответствии с наблюдавшейся частотой. Для описания частоты нежелательных реакций используется следующая классификация: очень часто (? 1/10); часто (? 1/100 до < 1/10); нечасто (? 1/1000 до < 1/100); редко (? 1/10000 до < 1/1000); очень редко (< 1/10000); частота неизвестна (не может быть оценена на основе имеющихся данных). Ввиду значительных различий между наблюдавшимися частотами возникновения определенных нежелательных реакций в зависимости от показаний, в таблице 1 частоты нежелательных реакций представлены отдельно для пациентов с почечными, сердечными и печеночными трансплантатами. Таблица 6. Перечень нежелательных реакций, которые наблюдались у пациентов, получающих ММФ, в клинических исследованиях и при пострегистрационном применении. Нежелательная реакция (MedDRA) Класс систем органов Почечный трансплантат Печеночный трансплантат Сердечный трансплантат Частота Частота Частота Инфекции и инвазии Бактериальные инфекции Очень часто Очень часто Очень часто Грибковые инфекции Часто Очень часто Очень часто Протозойные инфекции Нечасто Нечасто Нечасто Вирусные инфекции Очень часто Очень часто Очень часто Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы) Доброкачественное новообразование кожи Часто Часто Часто Лимфома Нечасто Нечасто Нечасто Лимфопролиферативное заболевание Нечасто Нечасто Нечасто Новообразование Часто Часто Часто Рак кожи Часто Нечасто Часто Нарушения со стороны крови и лимфатической системы Анемия Очень часто Очень часто Очень часто Парциальная красноклеточная аплазия (ПККА) Нечасто Нечасто Нечасто Нарушение функции костного мозга Нечасто Нечасто Нечасто Экхимоз Часто Часто Очень часто Лейкоцитоз Часто Очень часто Очень часто Лейкопения Очень часто Очень часто Очень часто Панцитопения Часто Часто Нечасто Псевдолимфома Нечасто Нечасто Часто Тромбоцитопения Часто Очень часто Очень часто Нарушения со стороны иммунной системы Гиперчувствительность Нечасто Часто Часто Гипогаммаглобулинемия Нечасто Очень редко Очень редко Нарушения метаболизма и питания Ацидоз Часто Часто Очень часто Гиперхолестеринемия Очень часто Часто Очень часто Гипергликемия Часто Очень часто Очень часто Гиперкалиемия Часто Очень часто Очень часто Гиперлипидемия Часто Часто Очень часто Гипокальциемия Часто Очень часто Часто Гипокалиемия Часто Очень часто Очень часто Гипомагниемия Часто Очень часто Очень часто Гипофосфатемия Очень часто Очень часто Часто Гиперурикемия Часто Часто Очень часто Подагра Часто Часто Очень часто Снижение массы тела Часто Часто Часто Психические нарушения Спутанность сознания Часто Очень часто Очень часто Депрессия Часто Очень часто Очень часто Бессонница Часто Очень часто Очень часто Ажитация Нечасто Часто Очень часто Тревожность Часто Очень часто Очень часто Патологическое мышление Нечасто Часто Часто Нарушения со стороны нервной системы Головокружение Часто Очень часто Очень часто Головная боль Очень часто Очень часто Очень часто Гипертонус Часто Часто Очень часто Парестезия Часто Очень часто Очень часто Сонливость Часто Часто Очень часто Тремор Часто Очень часто Очень часто Судороги Часто Часто Часто Дисгевзия Нечасто Нечасто Часто Нарушения со стороны сердца Тахикардия Часто Очень часто Очень часто Нарушения со стороны сосудов Артериальная гипертензия Очень часто Очень часто Очень часто Артериальная гипотензия Часто Очень часто Очень часто Лимфоцеле Нечасто Нечасто Нечасто Венозный тромбоз Часто Часто Часто Вазодилатация Часто Часто Очень часто Нарушения со стороны дыхательной системы, органов грудной клетки и средостения Бронхоэктаз Нечасто Нечасто Нечасто Кашель Очень часто Очень часто Очень часто Одышка Очень часто Очень часто Очень часто Интерстициальное заболевание легких Нечасто Очень редко Очень редко Плевральный выпот Часто Очень часто Очень часто Легочный фиброз Очень редко Нечасто Нечасто Желудочно-кишечные нарушения Вздутие живота Часто Очень часто Часто Боль в животе Очень часто Очень часто Очень часто Колит Часто Часто Часто Запор Очень часто Очень часто Очень часто Снижение аппетита Часто Очень часто Очень часто Диарея Очень часто Очень часто Очень часто Диспепсия Очень часто Очень часто Очень часто Эзофагит Часто Часто Часто Отрыжка Нечасто Нечасто Часто Метеоризм Часто Очень часто Очень часто Гастрит Часто Часто Часто Желудочно-кишечное кровотечение Часто Часто Часто Желудочно-кишечная язва Часто Часто Часто Гиперплазия десен Часто Часто Часто Кишечная непроходимость Часто Часто Часто Язвы ротовой полости Часто Часто Часто Тошнота Очень часто Очень часто Очень часто Панкреатит Нечасто Часто Нечасто Стоматит Часто Часто Часто Рвота Очень часто Очень часто Очень часто Нарушения со стороны печени и желчевыводящих путей Увеличение активности щелочной фосфатазы в крови Часто Часто Часто Увеличение активности лактатдегидрогеназы в крови Часто Нечасто Очень часто Увеличение активности «печеночных» ферментов Часто Очень часто Очень часто Гепатит Часто Очень часто Нечасто Гипербилирубинемия Часто Очень часто Очень часто Желтуха Нечасто Часто Часто Нарушения со стороны кожи и подкожных тканей Акне Часто Часто Очень часто Алопеция Часто Часто Часто Сыпь Часто Очень часто Очень часто Гипертрофия кожи Часто Часто Очень часто Нарушения со стороны мышечной, скелетной и соединительной ткани Артралгия Часто Часто Очень часто Мышечная слабость Часто Часто Очень часто Нарушения со стороны почек и мочевыводящих путей Увеличение уровня креатинина в крови Часто Очень часто Очень часто Увеличение уровня мочевины в крови Нечасто Очень часто Очень часто Гематурия Очень часто Часто Часто Нарушение функции почек Часто Очень часто Очень часто Общие нарушения и реакции в месте введения Астения Очень часто Очень часто Очень часто Озноб Часто Очень часто Очень часто Отек Очень часто Очень часто Очень часто Грыжа Часто Очень часто Очень часто Недомогание Часто Часто Часто Боль Часто Очень часто Очень часто Пирексия Очень часто Очень часто Очень часто Впервые возникший острый воспалительный синдром, связанный с ингибиторами синтеза пуринов Нечасто Нечасто Нечасто Описание отдельных нежелательных реакций Злокачественные новообразования У пациентов, которые получают комбинированную иммунодепрессивную терапию, в том числе ММФ, отмечается повышенный риск развития лимфом и других злокачественных новообразований, особенно новообразований кожи (см. раздел «Особые указания»). Трехлетние данные по безопасности у пациентов после пересадки почки или сердца не выявили каких-либо неожиданных изменений в показателе заболеваемости злокачественными новообразованиями по сравнению с годичными показателями. После пересадки печени пациентов наблюдали в течение 1-3 лет. Инфекции У всех пациентов, получающих иммунодепрессанты, риск бактериальных, вирусных и грибковых инфекций (некоторые из которых могут привести к летальному исходу), включая оппортунистические инфекции и латентную вирусную реактивацию, повышен. Риск возрастает с увеличением степени иммунодепрессии (см. раздел «Особые указания»). Наиболее серьезными инфекциями были сепсис, перитонит, менингит, эндокардит, туберкулез и атипичная микобактериальная инфекция. В контролируемых клинических исследованиях у пациентов, получающих ММФ (2 г или 3 г один раз в сутки) в комбинации с другими иммунодепрессантами после пересадки почки, сердца и печени, наиболее часто встречались оппортунистические инфекции, вызванные Candida mucocutaneous, цитомегаловирусная (ЦМВ) виремия/ЦМВ синдром и простой герпес (Herpes simplex). Пациентов наблюдали, как минимум, в течение 1 года после пересадки. Доля пациентов с ЦМВ виремией/синдромом составила 13,5 %. У пациентов, получавших иммунодепрессанты, в том числе ММФ, отмечались случаи нефропатии, ассоциированной с ВК-вирусом, а также прогрессирующей мультифокальной лейкоэнцефалопатии (ПМЛ), ассоциированной с JC-вирусом. Нарушения со стороны крови и лимфатической системы Цитопении, включая лейкопению, анемию, тромбоцитопению и панцитопению, являются установленным риском, связанным с применением ММФ, и могут привести или способствовать возникновению инфекций и кровотечений (см. раздел «Особые указания»). Отмечались агранулоцитоз и нейтропения; таким образом пациенты, получающие ММФ, должны находиться под регулярным наблюдением (см. раздел «Особые указания»). Также сообщалось о развитии апластической анемии и нарушении функции костного мозга у пациентов, получавших терапию ММФ, некоторые из этих случаев были с летальным исходом. У пациентов, получавших лечение ММФ, отмечались случаи ПККА (см. раздел «Особые указания»). Наблюдались отдельные случаи патологической морфологии нейтрофилов (включая приобретенную аномалию Пельгера-Хьюэта), не сопровождавшиеся нарушением функции нейтрофилов. Данные изменения могут свидетельствовать о сдвиге степени зрелости нейтрофилов влево в анализах крови, что может быть ошибочно расценено как признаки инфекции у пациентов с иммунодепрессией (как, например, у пациентов, получающих ММФ). Желудочно-кишечные нарушения Наиболее серьезными нарушениями со стороны ЖКТ были язвы и кровотечения, которые являются установленными рисками при применении ММФ. В опорных клинических исследованиях часто наблюдались язвы ротовой полости, желудка, кишечника, эзофагеальные и дуоденальные язвы, во многих случаях осложнявшиеся кровотечениями; наблюдались кровавая рвота, мелена и геморрагические формы гастрита и колита. Наиболее частыми нарушениями со стороны ЖКТ были диарея, тошнота и рвота. Эндоскопическое обследование пациентов с диареей, вызванной приемом ММФ, выявило отдельные случаи атрофии кишечных ворсинок (см. раздел «Особые указания»). Гиперчувствительность Отмечались реакции гиперчувствительности, включая ангионевротический отек и анафилактические реакции. Влияние на течение беременности, послеродовые и перинатальные состояния У пациенток, получавших ММФ, зарегистрированы случаи самопроизвольного выкидыша, в основном в I триместре беременности (см. раздел «Применение при беременности и в период грудного вскармливания»). Врожденные нарушения В пострегистрационном периоде отмечались случаи врожденных пороков развития у детей пациенток, принимавших ММФ во время беременности в комбинации с другими иммунодепрессантами (см. раздел «Применение при беременности и в период грудного вскармливания»). Нарушения со стороны дыхательной системы, органов грудной клетки и средостения У пациентов, получавших лечение ММФ в комбинации с другими иммунодепрессантами, зарегистрированы отдельные сообщения об интерстициальном заболевании легких и легочном фиброзе; некоторые из этих случаев были с летальным исходом. Кроме того, отмечались случаи бронхоэктаза у детей и взрослых. Нарушения со стороны иммунной системы У пациентов, получавших ММФ в комбинации с другими иммунодепрессантами, отмечалась гипогаммаглобулинемия. Общие нарушения и реакции в месте введения В опорных клинических исследованиях очень часто наблюдались отеки, включая периферические отеки, отеки лица и мошонки. Также очень часто отмечались случаи скелетно-мышечной боли, а именно миалгия, боли в шее и спине. Кроме того, в ходе пострегистрационного применения был описан впервые возникший острый воспалительный синдром, связанный с ингибиторами синтеза пуринов. Данный синдром описывался как парадоксальная провоспалительная реакция, вызванная ММФ и другими ингибиторами синтеза пуринов. Указанная реакция характеризуется лихорадкой, артралгиями, артритом, мышечной болью и повышением уровня воспалительных маркеров. Согласно обобщенным литературным отчетам после прекращения применения препарата отмечается быстрое улучшение состояния. Особые группы пациентов Пациенты детского возраста (от 3 месяцев до 18 лет) Тип нежелательных реакций и частота их возникновения в клиническом исследовании при пероральном приеме 600 мг/м2 ММФ 2 раза в сутки у детей в возрасте от 3 месяцев до 18 лет (n=100) с почечным трансплантатом в целом не отличались от таковых у взрослых пациентов, получавших препарат в дозе 1 г 2 раза в сутки. Однако, такие нежелательные реакции, связанные с лечением, как диарея, сепсис, лейкопения, анемия и инфекции отмечались у > 10% пациентов детского возраста и чаще встречались у детей, особенно в возрасте до 6 лет, по сравнению со взрослыми пациентами. В открытом исследовании у детей с трансплантатом печени и в доступных медицинских литературных источниках у детей с трансплантатом печени и сердца тип нежелательных реакций и частота их возникновения были сопоставимы с таковыми у детей и взрослых с почечным трансплантатом. Пациенты пожилого возраста Пациенты пожилого возраста (? 65 лет) могут в целом быть подвержены большему риску развития нежелательных реакций из-за иммунодепрессии. У пациентов пожилого возраста, получающих ММФ в рамках комбинированной иммунодепрессивной терапии, риск некоторых инфекций (включая тканевые инвазивные формы манифестной цитомегаловирусной инфекции), а также, возможно, желудочно-кишечных кровотечений и отека легких может быть выше, чем у пациентов более молодого возраста
- ПередозировкаДанные о передозировке ММФ были получены в клинических исследованиях и при пострегистрационном применении. В большинстве случаев данных о нежелательных явлениях не зарегистрировано. Если при передозировке наблюдались нежелательные явления, они совпадали с известным профилем безопасности препарата Ожидается, что передозировка ММФ вероятно приведет к чрезмерной иммуносупрессии (как следствие этого к повышению чувствительности к инфекциям) и угнетению костного мозга (см. раздел «Особые указания»). В случае развития нейтропении необходимо прервать лечение ММФ или уменьшить дозу (см. раздел «Особые указания»). МФК нельзя удалить из организма методом гемодиализа. Однако, при высоких концентрациях МФКГ в плазме (> 100 мкг/мл) небольшие его количества все-таки выводятся. Препараты, связывающие желчные кислоты, например, колестирамин, могут способствовать устранению МФК из организма, увеличивая его экскрецию.
- Применение при беременности и кормлении грудьюЖенщины с детородным потенциалом (контрацепция у мужчин и женщин) Женщины При применении препарата Микофенолата мофетил следует избегать наступления беременности. Таким образом, пациенткам с детородным потенциалом необходимо использовать как минимум один надежный метод контрацепции (см. раздел «Противопоказания») до начала терапии, во время терапии и в течение шести недель после прекращения терапии препаратом Микофенолата мофетил, если они не выбрали воздержание от половой жизни в качестве метода контрацепции. Предпочтительно использовать два дополняющих друг друга метода контрацепции одновременно. Мужчины Клинические данные о воздействии ММФ на отцовский организм ограничены и не содержат свидетельств о повышенном риске развития врожденных пороков или выкидыша вследствие приема ММФ отцом. МФК является мощным тератогеном. Неизвестно, присутствует ли МФК в сперме. Согласно расчетам, основанным на результатах исследований у животных, максимальное количество МФК, которое потенциально может быть передано женщине, настолько мало, что его влияние будет маловероятным. Исследования у животных показали генотоксичность ММФ в концентрациях, лишь немного превышающих терапевтические экспозиции у человека, поэтому риск генотоксического действия на сперматозоиды не может быть полностью исключен. Таким образом, рекомендуются следующие предупредительные меры: ведущим половую жизнь пациентам-мужчинам или половым партнершам пациентов-мужчин следует использовать надежные методы контрацепции во время лечения пациента-мужчины ММФ и как минимум в течение 90 дней после прекращения терапии. Пациентам-мужчинам с репродуктивным потенциалом должно быть известно о потенциальных рисках зачатия ребенка; их следует обсудить с квалифицированным медицинским специалистом. Беременность Применение ММФ противопоказано во время беременности, за исключением случаев отсутствия подходящей альтернативной терапии для профилактики отторжения трансплантата. Не следует начинать лечение до получения отрицательного результата теста на беременность, чтобы исключить непреднамеренное применение препарата во время беременности. Перед началом терапии пациенток с детородным потенциалом необходимо проинформировать о повышенном риске спонтанных абортов и врожденных пороков развития, и направить на консультацию по поводу предотвращения и планирования беременности. Перед началом терапии препаратом Микофенолата мофетил у пациенток с детородным потенциалом должны быть получены отрицательные результаты 2-х тестов на беременность при использовании методов анализа сыворотки или мочи с чувствительностью не менее 25 мМЕ/мл для исключения непреднамеренного воздействия ММФ на эмбрион. Рекомендуется проведение второго теста через 8-10 дней после первого теста. В случае трансплантации от умерших доноров, если возможность проведения двух отдельных тестов на беременность с интервалом 8-10 дней отсутствует (ввиду временных ограничений доступности трансплантата), первый тест на беременность должен быть проведен непосредственно перед началом терапии, а второй через 8-10 дней после первого. Повторные тесты на беременность должны проводиться в зависимости от клинических показаний (например, после сообщения о нарушении правил контрацепции). Результаты всех тестов на беременность необходимо обсудить с пациенткой. Пациентки должны быть проинформированы, что в случае наступления беременности им необходимо незамедлительно проконсультироваться с лечащим врачом. ММФ представляет собой вещество, оказывающее мощное тератогенное воздействие на человека, повышающее риск спонтанных абортов и возникновения врожденных пороков развития при его применении во время беременности: • Частота спонтанных абортов у пациенток, получавших ММФ, составила 45-49 %, в то время как у пациенток, получавших лечение другими иммунодепрессантами после трансплантации солидных органов, такой риск составляет 12-33 %. • Согласно опубликованным данным у 23-27 % живых новорожденных, которые подверглись воздействию ММФ в период внутриутробного развития, наблюдались врожденные пороки развития (по сравнению с частотой пороков развития у живых новорожденных 2-3% в общей популяции и приблизительно 4-5% у пациентов, перенесших трансплантацию солидных органов, получающих лечение другими иммунодепрессантами (не ММФ). У детей пациенток, получавших лечение ММФ в комбинации с другими иммунодепрессантами во время беременности, при пострегистрационном применении наблюдались врожденные пороки развития, включая множественные пороки развития. Наиболее часто отмечались следующие пороки развития: • аномалии развития уха (например, аномалия формы или отсутствие наружного уха), атрезия наружного слухового прохода (среднего уха); • пороки развития лица, такие как расщепленная губа, расщепленное небо, микрогнатия и гипертелоризм глазниц; • аномалии развития глаза (например, колобома); • аномалии сердца, такие как дефект межпредсердной и межжелудочковой перегородок; • пороки развития пальцев (например, полидактилия, синдактилия); • трахеоэзофагеальные пороки развития (например, атрезия пищевода); • пороки развития нервной системы (такие как незаращение дужек позвонков); • пороки развития почек. Отдельные сообщения о следующих пороках развития: • микрофтальм; • врожденная киста сосудистого сплетения; • агенез прозрачной перегородки; • агенез обонятельного нерва. Исследования на животных показали репродуктивную токсичность (см. раздел подраздел «Доклинические данные по безопасности» раздела «Фармакологические свойства»). Лактация Было показано, что у лактирующих крыс ММФ выделяется с молоком. Неизвестно, выделяется ли ММФ с грудным молоком у женщин. Препарат Микофенолата мофетил противопоказан в период грудного вскармливания в связи с риском развития серьезных нежелательных реакций на ММФ у детей, находящихся на грудном вскармливании (см. раздел «Противопоказания»). Фертильность ММФ не оказывал воздействия на фертильность самцов крысы при пероральном введении в дозах до 20 мг/кг/сутки. Системная экспозиция при такой дозе в 2-3 раза превышала клиническую экспозицию, наблюдаемую при приеме препарата в рекомендованной клинической дозе 2 г/сутки у пациентов после трансплантации почки, и в 1.3-2 раза превышала клиническую экспозицию, наблюдаемую при приеме препарата в рекомендованной клинической дозе 3 г/сутки у пациентов после трансплантации сердца. В исследованиях фертильности и репродуктивности самок крыс пероральное введение ММФ в дозе 4,5 мг/кг/сутки вызывало пороки развития (в том числе анофтальмию, агнатию и гидроцефалию) в первом поколении потомства без какого-либо токсического действия на мать. Системная экспозиция при такой дозе приблизительно в 0,5 раза превышала клиническую экспозицию, наблюдаемую при приеме препарата в рекомендованной клинической дозе 2 г/сутки у пациентов после трансплантации почки, и приблизительно в 0,3 раза превышала клиническую экспозицию, наблюдаемую при приеме препарата в рекомендованной клинической дозе 3 г/сутки у пациентов после трансплантации сердца. В последующих поколениях потомства влияния на фертильность или репродуктивность самок не отмечалось.
- Влияние на способность управлять транспортом и механизмамиММФ оказывает умеренное влияние на способность управлять транспортными средствами, механизмами. ММФ может вызывать сонливость, спутанность сознания, головокружение, тремор или артериальную гипотензию, таким образом, пациентам рекомендуется соблюдать осторожность при управлении транспортными средствами, механизмами.
- Особые указанияНовообразования Как и на фоне комбинированной иммунодепрессии вообще, так и при применении ММФ как компонента иммунодепрессивной схемы, имеется повышенный риск развития лимфом и других злокачественных новообразований, особенно кожи (см. раздел «Побочное действие»). Этот риск, по-видимому, связан не с применением какого-либо препарата как такового, а с интенсивностью и продолжительностью иммунодепрессии. Как и у всех пациентов с повышенным риском рака кожи, следует ограничить воздействие солнечных и ультрафиолетовых лучей ношением соответствующей закрытой одежды и использованием солнцезащитных кремов с высоким значением защитного фактора. Инфекции У пациентов, получающих иммунодепрессанты, включая ММФ, существует повышенный риск развития оппортунистических инфекций (бактериальных, грибковых, вирусных и протозойных), инфекций с летальным исходом и сепсиса (см. раздел «Побочное действие»). Подобные случаи включают реактивацию латентной вирусной инфекции, например, гепатита В или С, или инфекции, вызванной полиомавирусами (нефропатия, ассоциированная с ВК-вирусом, ПМЛ, ассоциированная с JC-вирусом). Сообщалось о случаях развития гепатита вследствие реактивации вирусов гепатита В или С у пациентов носителей вирусов гепатита В или С, получавших иммунодепрессивную терапию. Данные инфекции часто связаны с высокой общей иммунодепрессивной нагрузкой и могут приводить к серьезным нарушениям или к летальному исходу, что следует учитывать при проведении дифференциальной диагностики пациентов с иммунодепрессией и ухудшением функции почек или неврологическими симптомами. Поскольку МФК оказывает определенный цитостатический эффект на Т- и В-лимфоциты, течение COVID-19 может быть более тяжелым. У пациентов с клинически значимым COVID-19 в индивидуальном порядке следует рассмотреть снижение дозы или прекращение терапии ММФ, принимая во внимание риск отторжения у пациентов, перенесших трансплантацию. Необходим тщательный мониторинг риска отторжения. При применении ММФ в комбинации с другими иммунодепрессантами наблюдались случаи гипогаммаглобулинемии при рецидивирующих инфекциях. В некоторых из этих случаев переход с ММФ на альтернативный иммунодепрессант приводил к нормализации уровней IgG в сыворотке крови. У пациентов с рецидивирующими инфекциями, получающих ММФ, следует измерять уровень иммуноглобулинов в сыворотке крови. При устойчивой, клинически значимой гипогаммаглобулинемии следует рассмотреть возможность применения соответствующих клинических мер, с учетом возможных цитостатических эффектов, которые МФК оказывает на Т- и В-лимфоциты. Доступны опубликованные данные о развитии бронхоэктазов у взрослых и детей, которые получали ММФ, в комбинации с другими иммунодепрессантами. В некоторых из этих случаев переход с ММФ на другой иммунодепрессант приводил к снижению выраженности симптомов со стороны дыхательной системы. Риск развития бронхоэктазов может быть связан с гипогаммаглобулинемией или с прямым воздействием на легкие. Также получены отдельные сообщения об интерстициальном заболевании легких и легочном фиброзе, некоторые из которых были с летальным исходом (см. раздел «Побочное действие»). Рекомендуется обследовать пациентов со стойкими легочными симптомами, такими как кашель и одышка. Система крови и иммунная система За пациентами, получающими ММФ, необходимо наблюдать на предмет развития нейтропении, которая может быть связана как с приемом препарата, так и с применением других лекарственных препаратов, вирусными инфекциями или сочетаниями этих причин. При лечении ММФ необходимо определять развернутую формулу крови в течение первого месяца еженедельно, в течение второго и третьего месяцев лечения - два раза в месяц, а затем на протяжении первого года - ежемесячно. При возникновении нейтропении (абсолютное число нейтрофилов < 1,3х103/мкл) необходимо прервать лечение ММФ или уменьшить дозу и тщательно наблюдать пациента. Случаи развития парциальной красноклеточной аплазии (ПККА) наблюдались у пациентов, принимавших ММФ в комбинации с другими иммунодепрессивными препаратами. Механизм развития ПККА при применении ММФ не известен. В некоторых случаях ПККА может быть обратимой после снижения дозы ММФ или его отмены. Изменение терапии ММФ следует осуществлять только на фоне тщательного наблюдения за реципиентами трансплантата для минимизации риска его отторжения (см. раздел «Побочное действие»). Пациенты, получающие ММФ, должны быть проинструктированы о необходимости сразу же сообщать врачу о любых признаках инфекции, неожиданного возникновения гематом, кровотечений или других признаках нарушения функции костного мозга. Пациентов следует проинформировать, что в ходе лечения препаратом вакцинация может быть менее эффективной; необходимо избегать применения живых ослабленных вакцин (см. раздел «Взаимодействие с другими лекарственными средствами»). Важное значение может иметь вакцинация для профилактики гриппа. Врачи должны действовать в соответствии с национальными рекомендациями по проведению вакцинации против гриппа. Желудочно-кишечный тракт (ЖКТ) Прием ММФ сопровождался более высокой частотой нежелательных явлений со стороны ЖКТ, включая нечастые случаи изъязвления слизистой оболочки ЖКТ, желудочно-кишечные кровотечения, перфорации ЖКТ. Необходимо соблюдать осторожность при применении ММФ у пациентов с серьезными заболеваниями пищеварительного тракта в стадии обострения. ММФ является ингибитором инозинмонофосфатдегидрогеназы (ИМФДГ), поэтому его не следует применять у пациентов с редким генетически обусловленным наследственным дефицитом гипоксантингуанинфосфорибозилтрансфе¬разы (синдромы Леша-Найена и Келли-Зигмиллера). Взаимодействие Необходимо соблюдать осторожность при переходе с комбинированной терапии, включающей иммунодепрессанты, обладающие влиянием на печеночно-кишечную рециркуляцию МФК (например, циклоспорин), на терапию препаратами, лишенными данного эффекта, (например, такролимус, сиролимус и белатацепт) и наоборот. Данный переход может привести к изменению экспозиции МФК. Необходимо соблюдать осторожность при применении препаратов, оказывающих влияние на печеночно-кишечный цикл МФК, например, колестирамин, антибиотики, вследствие их способности снижать плазменную концентрацию и эффективность ММФ (см. раздел «Взаимодействие с другими лекарственными средствами»). Терапевтический лекарственный мониторинг МФК может быть целесообразным при переходе с одного препарата комбинированной терапии на другой (например, с циклоспорина на такролимус или наоборот) или для обеспечения надлежащей иммунодепрессии у пациентов с высоким иммунологическим риском (например, риск отторжения трансплантата, терапия антибиотиками, добавление или отмена взаимодействующего препарата). ММФ не рекомендуется применять одновременно с азатиоприном, поскольку их одновременный прием не изучался. Соотношение риска и пользы одновременного применения ММФ и сиролимуса не установлено (см. раздел «Взаимодействие с другими лекарственными средствами»). Особые группы пациентов У пациентов пожилого возраста может возрастать риск нежелательных явлений, например, некоторых инфекций (включая тканевые инвазивные формы манифестной цитомегаловирусной инфекции), а также, возможно, желудочно-кишечных кровотечений и отека легких по сравнению с более молодыми пациентами (см. раздел «Побочное действие»). Тератогенность ММФ является мощным тератогеном для человека. Отмечались случаи спонтанных абортов (с частотой от 45 % до 49 %) и врожденных пороков развития (расчетная частота от 23 % до 27 %) при применении ММФ во время беременности. Таким образом, применение ММФ противопоказано при беременности, за исключением случаев, когда приемлемая альтернатива для предотвращения отторжения трансплантата отсутствует. Пациенток с детородным потенциалом следует проинформировать о рисках и необходимости следовать рекомендациям, представленным в разделе «Применение при беременности и в период грудного вскармливания» (например, методы контрацепции, тестирование на беременность), перед началом, во время лечения и после прекращения терапии ММФ. Лечащему врачу следует убедиться, что женщина, принимающая ММФ, понимает риск нанесения вреда ребенку, необходимость в эффективной контрацепции, а также необходимость незамедлительной консультации с лечащим врачом, если вероятно наступление беременности. Контрацепция (см. раздел «Применение при беременности и в период грудного вскармливания») Поскольку надежные клинические данные указывают на высокий риск абортов и врожденных пороков развития при применении ММФ во время беременности, следует прилагать все усилия для того, чтобы избежать наступления беременности во время лечения. Таким образом, женщины с детородным потенциалом должны использовать как минимум один надежный метод контрацепции (см. раздел «Противопоказания») перед началом, во время лечения и в течение шести недель после прекращения терапии ММФ, если они не выбрали воздержание от половой жизни в качестве метода контрацепции. Предпочтительно использовать два взаимодополняющих метода контрацепции одновременно для минимизации возможности неэффективной контрацепции и наступления незапланированной беременности. Рекомендации по контрацепции для мужчин см. в разделе «Применение при беременности и в период грудного вскармливания». Дополнительные меры предосторожности Пациентам не следует быть донорами крови в период лечения и, как минимум, в течение 6 недель после последнего приема ММФ. Пациентам не следует быть донорами спермы в период лечения и, как минимум, в течение 90 дней после последнего приема ММФ
- ВзаимодействиеАцикловир При одновременном применении ММФ и ацикловира наблюдались более высокие концентрации ацикловира в плазме, чем при применении только ацикловира. Изменения показателей фармакокинетики МФКГ (а именно, повышение концентрации МФКГ на 8 %) были минимальными и не считаются клинически значимыми. Поскольку плазменные концентрации МФКГ, как и ацикловира, повышаются при почечной недостаточности, есть вероятность, что ММФ и ацикловир (или его пролекарства, например, валацикловир) конкурируют в отношении канальцевой секреции, что может приводить к дальнейшему повышению концентрации обоих лекарственных средств. Антациды и ингибиторы протонного насоса (ИПН) При совместном применении ММФ с антацидами (алюминия и магния гидроксид) и с ИПН (лансопразол и пантопразол) наблюдалось снижение концентрации МФК. Однако значительная разница между частотами отторжения трансплантата у пациентов, принимающих ММФ одновременно с препаратами ИПН и без таковых, отсутствовала. Данное заключение теоретически распространяется и на все антациды, так как при приеме магния и алюминия гидроксида одновременно с ММФ концентрация МФК снижается в гораздо меньшей степени, чем при одновременном приеме ММФ с ИПН. Лекарственные препараты, которые влияют на печеночно-кишечную циркуляцию (например, колестирамин, циклоспорин, антибиотики) Следует соблюдать осторожность при применении лекарственных препаратов, которые влияют на печеночно-кишечную циркуляцию, в силу их потенциала снижать эффективность ММФ. Колестирамин После применения разовой дозы ММФ 1,5 г у здоровых добровольцев, предварительно принимавших по 4 г колестирамина 3 раза в сутки на протяжении 4 дней, наблюдалось уменьшение AUCМФК на 40 % (см. разделы «Фармакокинетика» и «Особые указания»). Необходимо соблюдать осторожность при одновременном применении из-за возможности снижения эффективности ММФ. Циклоспорин ММФ не влияет на фармакокинетику циклоспорина. Однако, при прекращении одновременного применения циклоспорина следует ожидать увеличения AUCMФK ~30 %. Циклоспорин влияет на печеночно-кишечную рециркуляцию МФК, что может привести к снижению экспозиции МФК примерно на 30-50 % у пациентов после трансплантации почек, получающих ММФ и циклоспорин (по сравнению с пациентами, получающими сиролимус или белатацепт с аналогичными дозами ММФ (см. раздел «Особые указания»). Напротив, при переходе пациентов с терапии циклоспорином на терапию иммуносупрессантами, не влияющими на печеночно-кишечную рециркуляцию МФК, следует ожидать изменение экспозиции МФК. Антибиотики, приводящие к гибели бактерии, продуцирующие ?-глюкуронидазу в кишечнике (например, антибиотики из группы аминогликозидов, цефалоспоринов, фторхинолонов и пенициллинов), могут нарушать печеночно-кишечную рециркуляцию МФКГ/МФК, что, в свою очередь, может привести к снижению системной экспозиции МФК. Доступна информация о следующих антибиотиках. Ципрофлоксацин или амоксициллин в комбинации с клавулановой кислотой У пациентов после трансплантации почек в дни непосредственно после перорального приема ципрофлоксацина или амоксициллина в комбинации с клавулановой кислотой наблюдается снижение минимальной концентрации МФК на ~50 %. При продолжении антибактериальной терапии данный эффект снижается, а после прекращения терапии - исчезает в течение нескольких дней. Изменение минимальной концентрации может неадекватно отражать изменение суммарной экспозиции МФК. Таким образом, изменение дозы ММФ обычно не требуется при отсутствии клинических признаков дисфункции трансплантата. Однако, в ходе комбинированной терапии и в течение нескольких дней после завершения приема антибиотиков пациентам необходим тщательный клинический мониторинг. Норфлоксацин и метронидазол У здоровых добровольцев значимого взаимодействия при одновременном применении ММФ отдельно с норфлоксацином или метронидазолом не наблюдалось. После однократного применения ММФ в комбинации с норфлоксацином и метронидазолом экспозиция МФК снижалась на ~30 %. Триметоприм/сульфаметоксазол Влияния на биодоступность МФК не отмечалось. Лекарственные препараты, влияющие на глюкуронирование (исавуконазол и телмисартан) При одновременном применении с препаратами, ингибирующими глюкуронирование МФК, ее экспозиция может изменяться. Таким образом, при одновременном применении препарата Микофенолата мофетил с препаратами, влияющими на глюкуронирование, следует соблюдать осторожность. Исавуконазол При одновременном применении с исавуконазолом AUC0-? МФК увеличивалась на 35 %. Телмисартан Одновременное применение телмисартана с ММФ приводит к уменьшению концентрации МФК на ~30 %. Телмисартан оказывает влияние на выведение МФК путем увеличения экспрессии гамма рецептора, активируемого пероксисомными пролифераторами, что, в свою очередь увеличивает экспрессию и активность гена UGT1А9. Не было выявлено клинических проявлений фармакокинетического лекарственного взаимодействия при сравнении частоты отторжения трансплантата и профилей нежелательных явлений у пациентов, получающих ММФ с или без сопутствующей терапии телмисартаном. Ганцикловир По результатам исследования с однократным пероральным приемом рекомендованных доз ММФ и внутривенным введением ганцикловира с учетом известного влияния почечной недостаточности на фармакокинетику ММФ (см. раздел «Способ применения и дозы») и ганцикловира можно предположить, что одновременное применение этих двух препаратов (конкурирующих в процессе канальцевой секреции) приведет к повышению концентраций МФКГ и ганцикловира. Существенного изменения фармакокинетики МФК не ожидается, поэтому корректировать дозу ММФ не нужно. В случае применения ММФ и ганцикловира (или его пролекарства, например, валганцикловира) за пациентами с почечной недостаточностью следует тщательно наблюдать; также необходимо следовать рекомендациям по коррекции дозы ганцикловира. Пероральные контрацептивы При совместном применении ММФ и пероральных контрацептивов фармакокинетика и фармакодинамика последних не изменялась. Рифампицин У пациентов, которые не принимали циклоспорин, одновременный прием ММФ и рифампицина приводил к уменьшению экспозиции МФК на 18 %-70 % (AUC0-12). Рекомендуется контроль экспозиции МФК и коррекция дозы ММФ для поддержания клинического эффекта при совместном применении. Севеламер Одновременное применение севеламера и МФК у взрослых и детей снижало Cmax и AUC0-12 МФК на 30 % и 25 %, соответственно, без каких-либо клинических последствий (например, отторжения трансплантата). Тем не менее, рекомендуется принимать ММФ как минимум за один час до или через три часа после приема севеламера для минимизации воздействия на всасывание МФК. Данные в отношении применения ММФ совместно с препаратами, отличными от севеламера и связывающими фосфаты, отсутствуют. Такролимус У пациентов после пересадки печени, начавших терапию ММФ и такролимусом, не отмечалось значимого воздействия на AUC и Cmax МФК (активного метаболита ММФ). Напротив, у пациентов с печеночным трансплантатом после многократного приема ММФ в дозе 1,5 г 2 раза в сутки AUC такролимуса возрастала примерно на 20 %. У пациентов после трансплантации почек применение ММФ, по-видимому, не влияло на концентрацию такролимуса (см. раздел «Особые указания»). Живые ослабленные вакцины Живые ослабленные вакцины не должны вводиться пациентам в состоянии иммунодепрессии. Антителообразование в ответ на другие вакцины может быть снижено (см. раздел «Особые указания»). Возможные взаимодействия При одновременном применении пробенецида и ММФ у обезьян отмечалось увеличение AUC МФКГ в плазме в 3 раза. Таким образом, другие лекарственные средства, подвергающиеся канальцевой секреции, могут конкурировать с МФКГ, что приводит к увеличению концентрации МФКГ или другого препарата в плазме, который также подвергается канальцевой секреции. Дети Исследования взаимодействий проводились только у взрослых пациентов
- Страна-производительРоссия
- Количество в упаковке50
- УпаковкаТаблетки, покрытые пленочной оболочкой, 500 мг - 50 шт в уп., вместе с инструкцией по медицинскому применению (листок-вкладыш) помещают в картонную упаковку (пачку).
- Вес100
- Совместимость<p><em>Ацикловир</em></p> <p>При одновременном применении ММФ и ацикловира наблюдались более высокие концентрации МФКГ и ацикловира в плазме, чем при применении каждого препарата отдельно. Поскольку плазменные концентрации МФКГ, как и ацикловира, повышаются при почечной недостаточности, есть вероятность, что эти два препарата конкурируют в отношении канальцевой секреции, что может приводить к дальнейшему повышению концентрации обоих лекарственных средств.</p> <p><em>Антациды и ингибиторы протонного насоса (ИПН)</em></p> <p>При совместном применении ММФ с антацидами (алюминия и магния гидроксид) и с ингибиторами протонного насоса (лансопразол и пантопразол) наблюдалось снижение концентрации МФК. Однако значительная разница между частотами отторжения трансплантата у пациентов, принимающих ММФ одновременно с препаратами ИПН и без таковых, отсутствовала. Данное заключение теоретически распространяется и на антациды, так как при их приеме одновременно с ММФ концентрация МФК снижается в гораздо меньшей степени, чем при одновременном приеме ММФ с ИПН.</p> <p><em>Колестирамин</em></p> <p>После применения разовой дозы ММФ 1.5 г у здоровых добровольцев, предварительно принимавшим по 4 г колестирамина 3 раза в сутки на протяжении 4 дней, наблюдалось уменьшение AUC<img style="vertical-align: top; max-width: 100%; height: auto;" src="https://cdn.pharm-portal.ru/zgrwhhbxm889gykjvg34yx8a/public/documents/e1/73/72/f87fdf9df9349e53f7b03e5d91ab25e2c72145183ba6aece2392c30213.jpg" alt="" width="29" height="25" /> на 40%. Необходимо соблюдать осторожность при одновременном применении ММФ и препаратов, влияющих на печеночно-кишечную рециркуляцию (см. раздел «Особые указания»).</p> <p><em>Циклоспорин</em></p> <p>ММФ не влияет на фармакокинетику циклоспорина. Однако циклоспорин влияет на печеночно-кишечную рециркуляцию МФК, что может привести к увеличению AUC<img style="vertical-align: top; max-width: 100%; height: auto;" src="https://cdn.pharm-portal.ru/zgrwhhbxm889gykjvg34yx8a/public/documents/e1/73/72/f87fdf9df9349e53f7b03e5d91ab25e2c72145183ba6aece2392c30213.jpg" alt="" width="29" height="25" /> примерно на 30% при прекращении приема циклоспорина у пациентов после трансплантации почек, получающих ММФ и циклоспорин (по сравнению с пациентами, получающими сиролимус или белатацепт с аналогичными дозами ММФ). Напротив, при переходе пациентов с терапии циклоспорином на терапию иммунодепрессантами, не влияющими на печеночно-кишечную рециркуляцию МФК, следует ожидать изменение экспозиции МФК.</p> <p><em>Телмисартан</em></p> <p>Одновременное применение с ММФ приводит к уменьшению концентрации МФК примерно на 30%. Телмисартан оказывает влияние на выведение МФК путем увеличения экспрессии гамма рецептора, активируемого пероксисомными пролифераторами, что в свою очередь увеличивает экспрессию и активность гена UGT1А9. Не было выявлено клинических проявлений лекарственного взаимодействия при сравнении частоты отторжения трансплантата и профилей нежелательных явлений у пациентов, получающих ММФ с или без сопутствующей терапии телмисартаном.</p> <p><em>Ганцикловир</em></p> <p>По результатам исследования с однократным пероральным приемом рекомендованных доз ММФ и внутривенным введением ганцикловира с учетом известного влияния почечной недостаточности на фармакокинетику ММФ (см. разделы «Фармакокинетика в особых клинических случаях» и «Особые указания») и ганцикловира можно предположить, что одновременное применение этих двух препаратов (конкурирующих в процессе канальцевой секреции) приведет к повышению концентраций МФКГ и ганцикловира. Существенного изменения фармакокинетики МФК не ожидается, поэтому корректировать дозу ММФ не нужно. Если ММФ и ганцикловир (или его пролекарства, например, валганцикловир) применяют у пациентов с почечной недостаточностью, необходимо тщательно наблюдать пациентов.</p> <p><em>Пероральные контрацептивы</em></p> <p>ММФ не влияет на фармакокинетику пероральных контрацептивов. В исследовании при участии 18 женщин с псориазом при одновременном приеме на протяжении 3 менструальных циклов ММФ (1 г 2 раза в сутки) с комбинированными пероральными контрацептивами, содержащими этинилэстрадиол (0.02-0.04 мг) и левоноргестрел (0.05-0.2 мг), дезогестрел (0.15 мг) или гестоден (0.05-0.1 мг), не было выявлено клинически значимого воздействия ММФ на концентрации прогестерона, лютеинизирующего гормона (ЛГ) и фолликулостимулирующего гормона (ФСГ). Таким образом, ММФ не оказывает влияния на подавление овуляции под действием пероральных контрацептивов.</p> <p>Однако во время приема ММФ дополнительно к пероральным контрацептивам необходимо использовать и другие методы контрацепции (см. раздел «Применение при беременности и в период грудного вскармливания»).</p> <p><em>Такролимус</em></p> <p>При одновременном применении не выявлено влияния на AUC и максимальную концентрацию (С<img style="vertical-align: top; max-width: 100%; height: auto;" src="https://cdn.pharm-portal.ru/zgrwhhbxm889gykjvg34yx8a/public/documents/e4/ba/d6/28f9391b13a9c78d6f0f3117e6ca1fbbbe36fc28d050420532cb8d32a0.jpg" alt="" width="22" height="25" />) МФК у пациентов после пересадки печени и почек. У пациентов после трансплантации почек применение ММФ не влияло на концентрацию такролимуса. У пациентов со стабильным печеночным трансплантатом AUC такролимуса после многократного приема ММФ в дозе 1.5 г 2 раза в сутки возрастала примерно на 20%.</p> <p><em>Сиролимус</em></p> <p>У пациентов после трансплантации почек одновременный прием ММФ и циклоспорина приводил к уменьшению экспозиции МФК на 30-50% по сравнению с пациентами, получающими комбинацию сиролимуса и ММФ.</p> <p><em>Рифампицин</em></p> <p>После коррекции дозы отмечено уменьшение экспозиции МФК на 70% (AUC₀₋₁₂) у пациентов после одномоментной трансплантации сердца и легких, рекомендуется контроль экспозиции МФК и коррекция дозы ММФ для поддержания клинического эффекта при совместном применении.</p> <p><em>Антибиотики, приводящие к гибели бактерий, продуцирующих β-глюкуронидазу в кишечнике (например, антибиотики из группы аминогликозидов, цефалоспоринов, фторхинолонов и пенициллинов),</em> могут нарушать печеночно-кишечную рециркуляцию МФКГ/МФК, что, в свою очередь, может привести к снижению системной экспозиции МФК.</p> <p><em>Ципрофлоксацин и амоксициллин в комбинации с клавулановой кислотой</em></p> <p>У пациентов после трансплантации почек в дни непосредственно после перорального приема ципрофлоксацина или амоксициллина в комбинации с клавулановой кислотой наблюдается снижение минимальной концентрации МФК на 54%. При продолжении антибактериальной терапии данный эффект снижается, а после прекращения терапии - исчезает. Клиническое значение этого явления не известно, поскольку изменение минимальной концентрации может неадекватно отражать изменение суммарной экспозиции МФК.</p> <p><em>Норфлоксацин и метронидазол</em></p> <p>Применение норфлоксацина в комбинации с метронидазолом снижает AUС₀₋₄₈ МФК на 30% после однократного приема ММФ. При отдельном применении одного из этих антибиотиков такое влияние на системную экспозицию МФК отсутствует.</p> <p><em>Триметоприм/сульфаметоксазол</em></p> <p>При комбинированном применении с триметопримом/сульфаметоксазолом влияние на системную экспозицию МФК (AUC, C<img style="vertical-align: top; max-width: 100%; height: auto;" src="https://cdn.pharm-portal.ru/zgrwhhbxm889gykjvg34yx8a/public/documents/e4/ba/d6/28f9391b13a9c78d6f0f3117e6ca1fbbbe36fc28d050420532cb8d32a0.jpg" alt="" width="22" height="25" />) не отмечалось.</p> <p><em>Другие взаимодействия</em></p> <p>При одновременном применении <em>пробенецида</em> и ММФ обезьянами отмечалось увеличение AUC МФКГ в плазме в 3 раза. Таким образом, другие лекарственные средства, подвергающиеся канальцевой секреции, могут конкурировать с МФКГ, что приводит к увеличению концентрации МФКГ или другого препарата в плазме, который также подвергается канальцевой секреции.</p> <p><em>Севеламер</em></p> <p>Одновременное применение севеламера и МФК у взрослых и детей снижало С<img style="vertical-align: top; max-width: 100%; height: auto;" src="https://cdn.pharm-portal.ru/zgrwhhbxm889gykjvg34yx8a/public/documents/e4/ba/d6/28f9391b13a9c78d6f0f3117e6ca1fbbbe36fc28d050420532cb8d32a0.jpg" alt="" width="22" height="25" /> и AUC₀₋₁₂ МФК на 30% и 25%, соответственно. Севеламер и другие фосфатсвязывающие препараты, не содержащие кальций, должны применяться через 2 часа после приема ММФ, чтобы уменьшить влияние на всасывание МФК.</p> <p><em>Живые ослабленные вакцины</em></p> <p>Не должны вводиться пациентам в состоянии иммунодепрессии. Антителообразование в ответ на другие вакцины может быть снижено (см.раздел «Особые указания»).</p>
- Нижний порог температуры2
- Верхний порог температуры25
- ПоказанияПрепарат Микофенолата мофетил применяют в виде комбинированной терапии с циклоспорином и глюкокортикостероидами. Взрослые и дети с площадью поверхности тела > 1,25 м2 (примерный детский возраст старше 12 лет) для дозировки 250 мг и взрослые и дети с площадью поверхности тела 1,5 м2 (примерный детский возраст старше 14 лет) для дозировки 500 мг: • профилактика острого отторжения трансплантата у пациентов после аллогенной пересадки почки. Взрослые: • профилактика острого отторжения трансплантата у пациентов после аллогенной пересадки сердца; • профилактика острого отторжения трансплантата у пациентов после аллогенной трансплантации печени
- Выберите товары и добавьте их в корзину;
- Перейдите в раздел «Корзина» и нажмите «Оформить заказ»;
- Укажите ваши данные;
- Выберите способ доставки и укажите адрес;
- Выберите способ оплаты;
- Нажмите "Оформить заказ";
- В зависимости от варианта оплаты - оплатите заказ или дождитесь звонка оператора (при самовывозе);
Если возникли вопросы с оформлением заказа, пишите менеджерам в онлайн-чат.
Оплачивайте покупки удобным способом. В интернет-магазине доступно 4 варианта оплаты:
- Картой Онлайн. Оплата производится через защищенное соединение на странице банка. Мы не видим и не сохраняем данные Вашей карты. Сразу после оплаты вы получите чек об оплате на электронную почту.
- Картой или электронными деньгами через Яндекс.Кассу.
- Безналичный расчет (для юр. лиц)
- Наличными или картой при самовывозе из нашей аптеки в гор. Самара.
- Наличными Курьеру при доставке по Самаре.
- Лекарства можно получить и оплатить СТРОГО в нашей аптеке в гор. Самара - Ул. Солнечная, д. 16, оф. 2. Если у Вас в корзине будут лекарства, вы не сможете выбрать другой вариант доставки, а при выборе города, отличного от Самары, у Вас не будет никаких вариантов доставки.
-
Курьерская служба DPD. Только для разрешенных, согласно законодательства РФ, к доставке товаров. Доставка по России курьерской службой DPD. 1-2 дня Европейская часть России. До 5 дней Сибирь. До 12 дней Дальний Восток.
Мы доставим Ваш заказ за несколько дней по всей территории России курьерскими службами на дом или в пункт выдачи заказов. Цена доставки высчитывается при оформлении заказа автоматически.
Стоимость доставки:
- В пункты самовывоза: от 210 рублей (от 1 рабочего дня)
- Курьером: от 310 рублей (от 1 рабочего дня)
-
Почта России.Самая большая география доставки и самая низкая стоимость доставки, при этом сроки и качество обслуживания в последнее время заметно улучшились.
В крупных городах доступны варианты доставки "Курьер Онлайн" и "Посылка Онлайн" - самые быстрые сроки доставки и самая низкая стоимость.
Все крупные центральные города России от 210 рублей курьером на дом, либо 160 рублей в отделение.
Также Почта России доставляет в самые отдаленные города.
-
Курьерская доставка по гор. Самара
Вы можете заказать доставку товара с помощью курьера, который прибудет по указанному адресу ежедневно с 9.00 до 21.00. После поступления товара на склад, мы свяжемся с вами и предложим выбрать удобное время доставки. Уточним адрес.
Вы вскрываете упаковку при курьере, осматриваете на целостность и соответствие указанной комплектации.
Стоимость доставки начинается от 249 рублей, в зависимости от адреса доставки.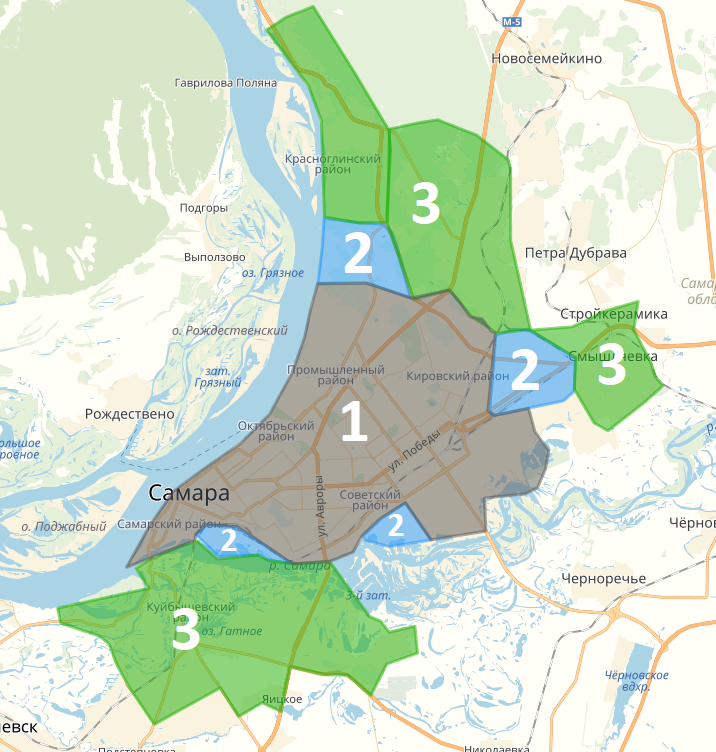
Зона 1 - 249 руб.
Зона 2 - 299 руб.
Зона 3 - 449 руб
Мы доставляем товары (кроме лекарств и товаров, требующих специальные условия перевозки) по всей России в короткие сроки. Рассчитать стоимость доставки вы можете на этой странице, нажав на кнопку "Рассчитать доставку".
Мы работаем с юридическими лицами по безналичному расчету. Предоставляем при этом все отчетные документы и сертификаты качества товара. Оформить заказ как юр. лицо, вы можете на странице оформления заказа.
Приобретать товар у нас очень выгодно - наши цены одни из самых низких во всем интернете. При этом, мы гарантируем, что вы получите товар высокого качества, ведь мы производим закупки у производителей, либо у федеральных фармацевтических дистрибьютеров.